题目内容
将一定量的锌与100 mL 18.5 mol/L的浓硫酸充分反应后,锌完全溶解,同时生成气体A 33.6 L(标准状况)。将反应后的溶液稀释至1 L,测得溶液中c(H+)=0.1 mol/L,则下列叙述中错误的是( )
A.反应中消耗的Zn的质量为97.5 g
B.气体A中SO2和H2的体积比为1∶4
C.反应中被还原的元素只有一种
D.反应中共转移电子3 mol
C
【解析】解答本题应注意以下两点:
(1)生成的33.6 L气体可能是SO2和H2的混合气体。
(2)假设反应的Zn一部分还原出SO2,一部分还原出H2,设未知数、列方程式计算。
设气体A中SO2、H2的物质的量分别为x、y。
则根据两个反应方程式可知
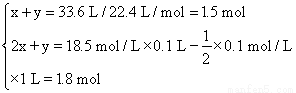
解得x=0.3 mol y=1.2 mol
消耗Zn的质量为(x+y)×65 g/mol=97.5 g,转移电子数为3 mol,被还原的元素有S、H两种。

练习册系列答案
 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案
相关题目







