题目内容
有机物A由碳、氢、氧三种元素组成,经测定其相对分子质量为90。现取1.8g A在纯氧中完全燃烧,将产物依次通过浓硫酸和碱石灰,浓硫酸增重1.08 g,碱石灰增重2.64 g。回答下列问题:
(1)1.8 g A中所含氢原子、碳原子的物质的量各是多少?
(2)通过计算确定该有机物的分子式。
(1)1.8 g A中所含氢原子、碳原子的物质的量各是多少?
(2)通过计算确定该有机物的分子式。
(1)n(H)=0.12mol n(C)=0.06mol
(2)C3H6O3
(2)C3H6O3
试题分析:利用燃烧法确定烃及烃的含氧衍生物的分子式时要注意守恒思想的应用:H2O中求H;CO2中求碳,有机物的总质量减C和H的质量得O质量,或者产物总氧减参加反应的氧气就是原来化合物的氧。浓硫酸增重1.08g是水,碱石灰增重2.64g是CO2,得n(H)=2x1.08/18=0.12(mol),m(H)=0.12(g);n(C)=2.64/44=0.06(mol),m(C)=0.72(g);n(O)=(1.8-0.12-0.72)/16=0.06(mol);C:H:O=0.06:0.12:0.06=1:2:1;最简式为 CH2O,其相对分子质量为90,分子式为C3H6O3。

练习册系列答案
 华东师大版一课一练系列答案
华东师大版一课一练系列答案
相关题目
 结构的物质) 。
结构的物质) 。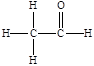 ,其PMR谱中有2个信号峰,其强度之比为3∶1。
,其PMR谱中有2个信号峰,其强度之比为3∶1。