题目内容
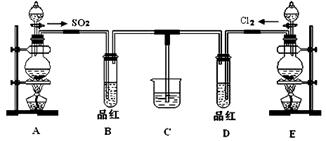
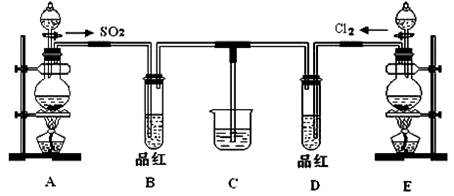
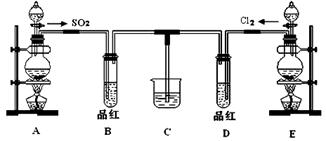
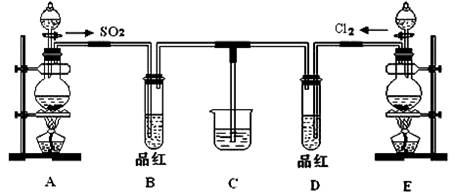
某化学实验小组同学为了证明、比较SO2和氯水的漂白性,设计了如下图所示的实验装置。
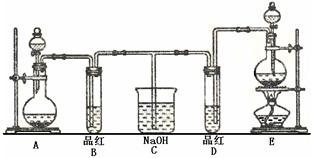
(1)实验室常选用制CO2的发生装置制SO2;实验室在用MnO2跟浓盐酸反应制备Cl2时,应选用上图A、E两发生装置中 ▲ 装置(填装置序号)制Cl2。在制Cl2的反应中浓盐酸所表现出的性质是 ▲ 。
(2)反应开始后,发现B、D两个试管中的品红溶液都褪去,停止通气后,给B、D两个
试管加热,两个试管中的现象分别为B: ▲ ,D: ▲ 。
(3)装置C的作用是 ▲ 。
(4)甲乙两名同学分别利用下图所示装置探究两种气体按不同比例混合后的漂白性。试分析:
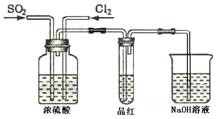
①在气体进入品红溶液之前,先将SO2和Cl2通过盛有浓硫酸装置的目的是: ▲ 。
②甲同学在实验过程中发现:通气一段时间后,品红溶液几乎不褪色,其原因是: ▲ ,并写出其相应的离子方程式: ▲ 。
③乙同学在实验过程中发现:通气一段时间后,品红溶液颜色随时间推移变得越来越浅,其原因是: ▲ 。
(1)E;还原性和酸性
(2)溶液由无色变成红色;溶液没有明显的变化
(3)保证安全,吸收多余的氯气和二氧化硫
(4)① 使两种气体充分混合;通过观察气泡的速度控制气体流量,使二者按一定比列混合。
②SO2和Cl2按1:1进气,二者恰好完全反应,生成无漂白性的H2SO4和HCl;
SO2 +Cl2 +2H2O===4H+ +SO42- +2Cl-
③SO2和Cl2的进气速度不相等,混合发生反应后其中一种气体有剩余,仍具有漂白性。
解析:

练习册系列答案
 名师导航单元期末冲刺100分系列答案
名师导航单元期末冲刺100分系列答案 名校名卷单元同步训练测试题系列答案
名校名卷单元同步训练测试题系列答案
相关题目