题目内容
某无色溶液X,由Na+、Ag+、Ba2+、Al3+、Fe3+、AlO2-、CO32-、SO42-中的若干种离子组成,取该溶液进行如下实验:
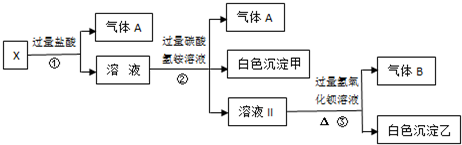
(1)气体A的成分是
(2)写出步骤①发生反应的所有离子方程式
(3)写出步骤②形成白色沉淀甲的离子方程式
(4)通过上述实验,可确定X溶液中一定存在的离子是

(1)气体A的成分是
CO2
CO2
(填化学式,下同),气体B的成分是NH3
NH3
.(2)写出步骤①发生反应的所有离子方程式
CO32-+2H+═H2O+CO2↑
CO32-+2H+═H2O+CO2↑
.(3)写出步骤②形成白色沉淀甲的离子方程式
AlO2-+4H+═Al3++2H2O,Al3++3HCO3-═Al(OH)3↓+3CO2↑
AlO2-+4H+═Al3++2H2O,Al3++3HCO3-═Al(OH)3↓+3CO2↑
.(4)通过上述实验,可确定X溶液中一定存在的离子是
CO32-,AlO2-,Na+
CO32-,AlO2-,Na+
,尚未确定是否存在的离子是SO42-
SO42-
,只要设计一个简单的后续实验就可以确定该离子是否存在,该方法是向所得沉淀乙中滴加足量的稀硝酸,若沉淀不完全溶解,则证明含有SO42-
向所得沉淀乙中滴加足量的稀硝酸,若沉淀不完全溶解,则证明含有SO42-
.分析:溶液呈无色,则不含Fe3+,加入过量盐酸只产生气体,则一定含有CO32-,不含Ag+,反应后溶液呈酸性,加入过量碳酸氢铵溶液,生成气体和白色沉淀,则发生反应应为:Al3++3HCO3-═Al(OH)3↓+3CO2↑,则原溶液中含有AlO2-,则一定不含Ba2+、Al3+、Fe3+,因这些离子与AlO2-发生相互促进的水解而不能大量共存,根据溶液电中性原则,一定含有Na+,最后加入过量氢氧化钡溶液,因之前加入的碳酸氢铵过量,则生成的白色沉淀可能为BaCO3,不能确定SO42-是否存在.
解答:解:溶液呈无色,则不含Fe3+,加入过量盐酸只产生气体,则一定含有CO32-,不含Ag+,反应后溶液呈酸性,加入过量碳酸氢铵溶液,生成气体和白色沉淀,则发生反应应为:Al3++3HCO3-═Al(OH)3↓+3CO2↑,则原溶液中含有AlO2-,则一定不含Ba2+、Al3+、Fe3+,因这些离子与AlO2-发生相互促进的水解而不能大量共存,根据溶液电中性原则,一定含有Na+,最后加入过量氢氧化钡溶液,因之前加入的碳酸氢铵过量,则生成的白色沉淀可能为BaCO3,不能确定SO42-是否存在.
(1)气体A的成分是CO2,所涉及反应有:CO32-+2H+═H2O+CO2↑,Al3++3HCO3-═Al(OH)3↓+3CO2↑,气体B为NH3,所涉及反应为:NH4++OH-=NH3↑+H2O,故答案为:CO2;NH3;
(2)溶液加入过量盐酸只产生气体,则一定含有CO32-,发生反应为:CO32-+2H+═H2O+CO2↑,故答案为:CO32-+2H+═H2O+CO2↑;
(3)溶液中含有AlO2-,加入过量盐酸发生反应:AlO2-+4H+═Al3++2H2O,加入过量碳酸氢铵溶液,生成气体和白色沉淀,则发生反应应为:Al3++3HCO3-═Al(OH)3↓+3CO2↑,故答案为:AlO2-+4H+═Al3++2H2O,Al3++3HCO3-═Al(OH)3↓+3CO2↑;
(4)由以上分析可知,X溶液中一定存在的离子是CO32-,AlO2-,Na+,因最后加入过量氢氧化钡溶液,因之前加入的碳酸氢铵过量,则生成的白色沉淀可能为BaCO3,不能确定SO42-是否存在,可向所得沉淀乙中滴加足量的稀硝酸,若沉淀不完全溶解,则证明含有SO42-,
故答案为:CO32-,AlO2-,Na+;SO42-;向所得沉淀乙中滴加足量的稀硝酸,若沉淀不完全溶解,则证明含有SO42-.
(1)气体A的成分是CO2,所涉及反应有:CO32-+2H+═H2O+CO2↑,Al3++3HCO3-═Al(OH)3↓+3CO2↑,气体B为NH3,所涉及反应为:NH4++OH-=NH3↑+H2O,故答案为:CO2;NH3;
(2)溶液加入过量盐酸只产生气体,则一定含有CO32-,发生反应为:CO32-+2H+═H2O+CO2↑,故答案为:CO32-+2H+═H2O+CO2↑;
(3)溶液中含有AlO2-,加入过量盐酸发生反应:AlO2-+4H+═Al3++2H2O,加入过量碳酸氢铵溶液,生成气体和白色沉淀,则发生反应应为:Al3++3HCO3-═Al(OH)3↓+3CO2↑,故答案为:AlO2-+4H+═Al3++2H2O,Al3++3HCO3-═Al(OH)3↓+3CO2↑;
(4)由以上分析可知,X溶液中一定存在的离子是CO32-,AlO2-,Na+,因最后加入过量氢氧化钡溶液,因之前加入的碳酸氢铵过量,则生成的白色沉淀可能为BaCO3,不能确定SO42-是否存在,可向所得沉淀乙中滴加足量的稀硝酸,若沉淀不完全溶解,则证明含有SO42-,
故答案为:CO32-,AlO2-,Na+;SO42-;向所得沉淀乙中滴加足量的稀硝酸,若沉淀不完全溶解,则证明含有SO42-.
点评:本题考查常见离子的检验及离子组成分的确定,题目难度中等,注意常见离子的检验方法,把握有关离子的性质,会书写反应的离子的方程式.

练习册系列答案
 备战中考寒假系列答案
备战中考寒假系列答案
相关题目

 、CO
、CO 1)气体A的成分是:_________________,气体B的成分是_____________
1)气体A的成分是:_________________,气体B的成分是_____________