题目内容
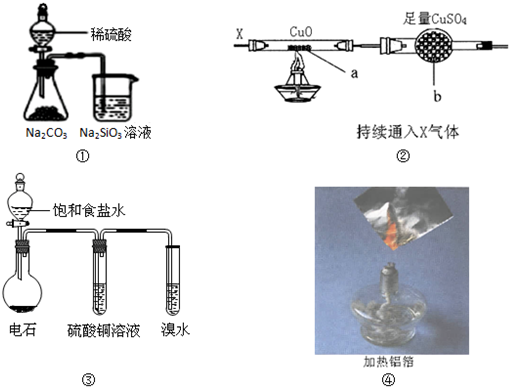
关于下列图示的说法正确的是

- A.图①所示实验不能比较硫、碳、硅三种元素的非金属性强弱
- B.图②a处有红色物质生成,b处变蓝,则X气体一定是H2
- C.图③所示实验装置中CuSO4溶液可用于除去杂质
- D.图④所示实验可观察到铝箔失去光泽,铝熔化并滴落
C
分析:A.由发生的反应可知,酸性为硫酸>碳酸>硅酸,利用最高价含氧酸的酸性比较非金属性的强弱;
B.b处变蓝,说明有水生成,a处有红色物质生成,则CuO被还原,X可能为氢气、乙醛、氨气等;
C.实验水和电石反应生成的乙炔中混有硫化氢,乙炔与硫酸铜溶液不反应,而硫化氢与硫酸铜溶液反应生成沉淀;
D.反应生成的氧化铝的熔点高,不会滴落.
解答:A.由发生的反应可知,酸性为硫酸>碳酸>硅酸,由最高价含氧酸的酸性可知,非金属性为S>C>Si,故A错误;
B.b处变蓝,说明有水生成,a处有红色物质生成,则CuO被还原,X可能为氢气、乙醛、氨气等,不一定为氢气,故B错误;
C.实验水和电石反应生成的乙炔中混有硫化氢,乙炔与硫酸铜溶液不反应,而硫化氢与硫酸铜溶液反应生成沉淀,则图③所示实验装置中CuSO4溶液可用于除去杂质,故C正确;
D.反应生成的氧化铝的熔点高,实验中可观察到铝箔失去光泽,铝熔化但不会滴落,故D错误;
故选C.
点评:本题考查化学实验方案的评价,涉及酸性和非金属的比较、除杂、物质的性质等,侧重物质性质的考查,选项B为解答的易错点,题目难度中等.
分析:A.由发生的反应可知,酸性为硫酸>碳酸>硅酸,利用最高价含氧酸的酸性比较非金属性的强弱;
B.b处变蓝,说明有水生成,a处有红色物质生成,则CuO被还原,X可能为氢气、乙醛、氨气等;
C.实验水和电石反应生成的乙炔中混有硫化氢,乙炔与硫酸铜溶液不反应,而硫化氢与硫酸铜溶液反应生成沉淀;
D.反应生成的氧化铝的熔点高,不会滴落.
解答:A.由发生的反应可知,酸性为硫酸>碳酸>硅酸,由最高价含氧酸的酸性可知,非金属性为S>C>Si,故A错误;
B.b处变蓝,说明有水生成,a处有红色物质生成,则CuO被还原,X可能为氢气、乙醛、氨气等,不一定为氢气,故B错误;
C.实验水和电石反应生成的乙炔中混有硫化氢,乙炔与硫酸铜溶液不反应,而硫化氢与硫酸铜溶液反应生成沉淀,则图③所示实验装置中CuSO4溶液可用于除去杂质,故C正确;
D.反应生成的氧化铝的熔点高,实验中可观察到铝箔失去光泽,铝熔化但不会滴落,故D错误;
故选C.
点评:本题考查化学实验方案的评价,涉及酸性和非金属的比较、除杂、物质的性质等,侧重物质性质的考查,选项B为解答的易错点,题目难度中等.

练习册系列答案
 全能测控一本好卷系列答案
全能测控一本好卷系列答案
相关题目
关于下列图示的说法正确的是( )
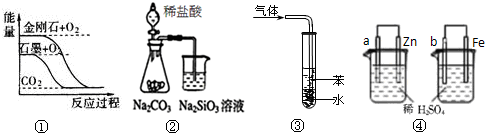

| A、图①表示石墨转变为金刚石是吸热反应 | B、图②所示实验可比较非金属性强弱:氯>碳>硅 | C、图③吸收NH3并防倒吸 | D、图④两装置中金属电极a、b都有气体产生,可判断金属活动性:a<b |