题目内容
19.分子式为C5Hl003且等量的该有机物分别与足量的NaHC03溶液、Na反应时产生的气体在相同条件下的体积比为1:1的同分异构体共有(不考虑立体异构)( )| A. | 4 | B. | 8 | C. | 12 | D. | 16 |
分析 有机物分子式为C5H10O3,等量的有机物与足量的NaHCO3溶液、Na反应时产生的气体在相同条件下的体积比为1:1,说明有机物分子中含有1个-COOH、1个-OH,该有机物可以看作,C4H10中2个H原子,分别被-COOH、-OH代替,结合C4H10的同分异构体判断.
解答 解:有机物分子式为C5H10O3,等量的有机物与足量的NaHCO3溶液、Na反应时产生的气体在相同条件下的体积比为1:1,说明有机物分子中含有1个-COOH、1个-OH,该有机物可以看作,C4H10中2个H原子,分别被-COOH、-OH代替,
若C4H10为正丁烷:CH3CH2CH2CH3,2个H原子分别被-COOH、-OH代替,都取代同一碳原子上2个H原子,有2种,取代不同C原子的2个H原子,有6种,相应的同分异构体有8种;
若C4H10为异丁烷:CH3CH(CH2)CH3,2个H原子分别被-COOH、-OH代替,都取代同一碳原子上2个H原子,有1种,取代不同C原子的2个H原子,有3种,相应的同分异构体有4种;
故该有机物的可能的结构有8+4=12种,
故选C.
点评 本题主要考查同分异构体的书写,判断有机物含有的官能团是关键,注意取代中利用定一移二进行判断.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
8.某有机物Z具有较广泛的抗菌作用,其生成机理可由X与Y相互作用:
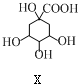 $→_{一定条件}^{Y}$
$→_{一定条件}^{Y}$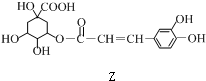
下列有关叙述中不正确的是( )
 $→_{一定条件}^{Y}$
$→_{一定条件}^{Y}$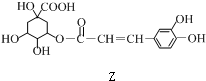
下列有关叙述中不正确的是( )
| A. | X分别与足量的Na、NaOH反应,消耗两者的物质的量之比为5﹕1 | |
| B. | Y的分子式为C9H8O3 | |
| C. | 1 mol Z与浓溴水反应最多消耗4molBr2 | |
| D. | 1 mol Z与足量NaOH溶液反应,最多消耗4mol NaOH |
10.大气污染再次成为今年“两会”的热门议题.下列做法不能改善大气环境的是( )
| A. | 大力开发新能源和可再生能源 | |
| B. | 城市大力发展轨道交通,少开私家车 | |
| C. | 清洁燃煤、提高燃油品质 | |
| D. | 学校、家庭安装空气净化装置 |
4.短周期元素X、Y、Z、W的原子序数依次增大,且原子最外层电子数之和为13.X与W同主族,Z是地壳中含量最高的元素.下列说法正确的是( )
| A. | 原子半径的大小顺序:r(Y)>r(Z)>r(W) | |
| B. | X和Y两元素一定不在同一周期 | |
| C. | 元素Z、W的简单离子的电子层结构相同 | |
| D. | X、W两元素一定能形成两种组成不同的氧化物 |
11.化学中有“四同”,根据“四同”的概念,下列物质间关系正确的是( )
| A. | 1H2、2H2--同位素 | B. | HCOOCH3、CH3OCHO--同分异构体 | ||
| C. | S2-、S22---同素异形体 | D. | 甲基丙烯酸、油酸--同系物 |
8.设NA表示阿伏加德罗常数的数值,下列叙述正确的是( )
| A. | 常温常压下,2.8gN2与C2H4的混合气体中含有的电子数为1.4NA | |
| B. | 标准状况下,1.12L NO与1.12LO2的混合物中含有的原子数为0.2NA | |
| C. | 25℃时,pH=13的Ba(OH)2溶液中含有的OH-数目为0.1NA | |
| D. | 常温下,1L0.1mol•L-1的NH4NO3溶液中氧原子数为0.3NA |
9.下列说法正确的是( )
| A. | 常温下,反应4Fe(OH)2(s)+2H2O(l)+O2(g)═4Fe(OH)3(s)能自发进行,证明该反应的△H<0 | |
| B. | 常温下,BaSO4分别在相同物质的量浓度的Na2SO4溶液和Al2(SO4)3溶液中的溶解度相同 | |
| C. | 常温下,向饱和Na2CO3溶液中加少量BaSO4粉末,过滤,向洗净的沉淀中加稀盐酸,有气泡产生,说明常温下Ksp(BaCO3)<Ksp(BaSO4) | |
| D. | 等体积、等物质的量浓度的NH3•H2O溶液与NH4Cl溶液混合后溶液呈碱性,说明NH3•H2O的电离程度小于NH${\;}_{4}^{+}$的水解程度 |
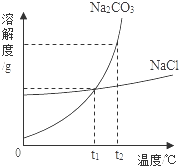 我国化学家侯德榜创立的侯氏制碱法,就是以海水晒盐得到的氯化钠为原料,制得纯碱碳酸钠,碳酸钠和氯化钠的溶解度曲线如图所示,试回答下列问题:
我国化学家侯德榜创立的侯氏制碱法,就是以海水晒盐得到的氯化钠为原料,制得纯碱碳酸钠,碳酸钠和氯化钠的溶解度曲线如图所示,试回答下列问题: