题目内容
如下图所示,甲、乙、丙、丁四种单质两两反应生成X、Y、Z、W四种化合物,已知: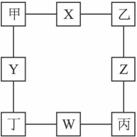
①甲、乙、丙、丁均为短周期元素形成的单质,常温下甲、乙、丙为气体,丁为中学化学中常见的金属单质。
②甲中所含元素的核电荷数是乙、丙所含元素的核电荷数之和。
③丁中所含元素原子的最外层电子数是乙中所含元素原子的最外层电子数的2倍。
④常温下,X是无色液体,Z是刺激性气体,X与W的反应能生成Z及另一种白色沉淀。
试回答:
(1)Y的化学式是______________,丙的电子式为______________。
(2)X与W反应的化学方程式是_______________________________________________。
(3)常温下某Z的水溶液的pH等于11,则该溶液中由水电离产生的OH-的物质的量浓度为______________。
(4)已知
(1)MgO ∶N┇┇N∶
(2)Mg3N2+6H2O====3Mg(OH)2↓+2NH3↑
(3)1×10-11 mol/L
(4)2H(g)+O2(g)====2H2O(l);ΔH=-571.6 kJ/mol
解析:常温下呈气态的单质可能是H2、O2、N2、Cl2。X是无色液体化合物应为H2O,则应有气体H2、O2,又甲、乙、丙能两两反应,另一种气体应是N2,那么Z为NH3。由②知甲为O2,氢原子最外层电子数为1,结合③知乙为H2,丁为Mg。由④知W为Mg3N2,其与H2O反应生成NH3和白色沉淀Mg(OH)2。

(15分)、如下图所示,甲、乙两池电极材料都是铁棒与碳棒,乙池中电子电子流动方向见图,回答下列问题:
(1)若两池中均盛200mL饱和NaCl溶液和酚酞的混合液,反应开始后:
①甲池中 极,乙池中的
极附近溶液变红(填“正”或“负”或“阴”或“阳”)。
②甲池碳极上电极反应式是
乙池中Fe电极上反应式为 。
③若乙池中收集到1.12L(标况下)有色气体时,停止实验,忽略池中溶液体积的变化,则池中溶液的c(OH—)约为 ,要使溶液恢复到电解前的相同的状况,应向溶液中补充一定量的 
| A.盐酸 | B.NaCl固体 | C.NaCl溶液 | D.HCl气体 |
①反应一段时间后,有红色物质析出的是甲池中的 棒,乙池中的 棒。
②写出乙池通电时总反应的离子方程式: 。
③若乙池中通过1.2mol 电子后停止实验,则乙池中共可收集到气体的体积为(标准状况下)

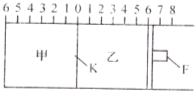 Ⅰ.如下图所示,甲、乙之间的隔板K和活塞F都可左右自由移动,甲充入2molA和1molB,乙中充入2molC和1molHe,只有A为有色气体,此时K停在O处.在一定条件下发生逆反应:2A(g)+B(g)?2C(g)△H<0;反应达到平衡后,再恢复至原温度.回答下列问题:
Ⅰ.如下图所示,甲、乙之间的隔板K和活塞F都可左右自由移动,甲充入2molA和1molB,乙中充入2molC和1molHe,只有A为有色气体,此时K停在O处.在一定条件下发生逆反应:2A(g)+B(g)?2C(g)△H<0;反应达到平衡后,再恢复至原温度.回答下列问题:
