题目内容
二氧化氯(ClO2)作为一种高效强氧化剂已被联合国世界卫生组织(WHO)列为AI级安全消毒剂.常温下二氧化氯为黄绿色或橘黄色气体,性质非常不稳定,温度过高或水溶液中ClO2的质量分数高于30%等均有可能引起爆炸,易与碱液反应生成盐和水.
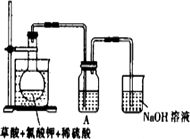
(1)某研究小组设计如图所示实验制备ClO2溶液,其反应的化学方程式为
2KClO3+H2C2O4+2H2SO4![]() 2KHSO4+2ClO2↑+2CO2↑+2H2O
2KHSO4+2ClO2↑+2CO2↑+2H2O
①在反应开始之前将烧杯中的水加热到80℃,然后停止加热,并使其温度保持在60~80℃之间.控制温度的目的是________________,图示装置中缺少的一种必须的玻璃仪器是________________
②装置A用于溶解产生的二氧化氯气体,其中最好盛放________(填字母).
A.20 mL 60℃的温水
B.100 mL冰水
C.100 mL饱和食盐水
D.100 mL沸水
③在烧瓶中加入12.25 g KClO3和9 g草酸(H2C2O4),然后再加入足量的稀硫酸,水浴加热,反应后生成ClO2的质量为________
(2)用ClO2处理过的饮用水(pH为5.5~6.5)常含有一定量对人体不利的亚氯酸根离子(ClO![]() ).饮用水中ClO2、ClO
).饮用水中ClO2、ClO![]() 的含量可用连续碘量法进行测定,实验步骤如下:
的含量可用连续碘量法进行测定,实验步骤如下:
步骤1:准确量取一定体积的水样加入锥形瓶中;
步骤2:调节水样的pH至7.0~8.0;
步骤3:加入足量的KI晶体;
步骤4:加入少量指示剂,用一定浓度的Na2S2O3溶液滴定至终点;
步骤5:再调节溶液的pH≤2.0;
步骤6:继续用相同浓度的Na2S2O3溶液滴定至终点.
①步骤1中若要量取20.00 mL水样,则应选用的仪器是________________
②步骤1~4的目的是测定水样中ClO2的含量,其反应的化学方程式为:
2ClO2+2KI![]() 2KClO2+I2,2Na2S2O3+I2
2KClO2+I2,2Na2S2O3+I2![]() Na2S4O6+2NaI,则步骤4中加入的指示剂为________________,滴定达到终点时溶液的颜色变化为________________
Na2S4O6+2NaI,则步骤4中加入的指示剂为________________,滴定达到终点时溶液的颜色变化为________________
③步骤5的目的是使I-将溶液中的ClO![]() 还原为Cl-以测定其含量,该反应的离子方程式为:________
还原为Cl-以测定其含量,该反应的离子方程式为:________
④若饮用水中ClO![]() 的含量超标,可向其中加入适量的Fe2+将ClO
的含量超标,可向其中加入适量的Fe2+将ClO![]() 还原为Cl-,则该反应的氧化产物为________(填化学式)
还原为Cl-,则该反应的氧化产物为________(填化学式)


 NCl3+3H2↑;假设NCl3中氮元素为+3价。
NCl3+3H2↑;假设NCl3中氮元素为+3价。