题目内容
物质的量为0.10 mol的镁条在只含有CO2和O2混合气体的容器中燃烧(产物不含碳酸镁),反应后容器内固体物质的质量不可能为
| A.3.2 g | B.4.0 g | C.4.2 g | D.4.6 g |
D
发生的反应有:
 ①
①
 ②
②
若0.10 mol镁条全部参与反应①,反应后固体的质量m=0.10 mol×40 g·mol-1=4.0 g。若0.10 mol镁条全部参与反应②,反应后固体的质量m=0.10 mol×40 g·mol-1+0.05 mol×12 g·mol-1=4.6 g。若CO2和O2的量不足,Mg条不能完全燃烧,则反应后固体的质量可能小于4.0 g,但不会等于或大于4.6 g,故D项错误。
 ①
① ②
②若0.10 mol镁条全部参与反应①,反应后固体的质量m=0.10 mol×40 g·mol-1=4.0 g。若0.10 mol镁条全部参与反应②,反应后固体的质量m=0.10 mol×40 g·mol-1+0.05 mol×12 g·mol-1=4.6 g。若CO2和O2的量不足,Mg条不能完全燃烧,则反应后固体的质量可能小于4.0 g,但不会等于或大于4.6 g,故D项错误。

练习册系列答案
 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案
相关题目
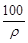 mL
mL