题目内容
16.PCl5的热分解反应如下:PCl5(g)![]() PCl3(g) + Cl2(g)
PCl3(g) + Cl2(g)
(1) 写出反应的平衡常数表达式;
(2) 已知某温度下,在容积为10.0L的密闭容器中充入2.00mol PCl5,达到平衡后,测得容器内PCl3的浓度为0.150mol/L。计算该温度下的平衡常数。
(1)K=![]() 或K=
或K=![]()
(2)K=![]()
解析:本题考查平衡常数及其计算,由反应方程式PCl5(g) ![]() PCl3(g)+Cl2(g)?
PCl3(g)+Cl2(g)?
K=![]() ;c(PCl5)的起始浓度为
;c(PCl5)的起始浓度为![]() =0.200 mol·L-1;平衡时
=0.200 mol·L-1;平衡时
c (PCl5)=0.200 mol·L-1-0.150 mol·L-1=0.050 0 mol·L-1??
c (Cl2)= c (PCl3)=0.150 mol·L-1;?
K= ![]() =
=![]() =0.45
=0.45

练习册系列答案
相关题目
 PCl3(g) + Cl2(g)。
PCl3(g) + Cl2(g)。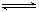 PCl3(g)
+ Cl2(g)。
PCl3(g)
+ Cl2(g)。