题目内容
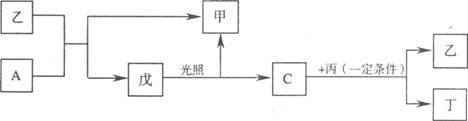
( 12分)A、B、C、D四种元素,A单质在B单质中燃烧发出苍白色火焰,C单质跟A、B形成的化合物的水溶液反应生成A单质,C原子与B原子的电子层数相同,且最外层电子数之差为奇数,D原子最外层电子数为K层电子数的3倍,其单质为淡黄色固体。
(1)四种元素符号为:A____________,B____________,C____________,D____________;
(2)离子的电子层结构相同的两种元素是______与_____,离子的结构示意图分别为____________、________________;
(3)A、B、C、D原子形成的最高价氧化物的化学式分别为__________、__________、__________、__________。
【解析】A单质在B单质中燃烧发出苍白色火焰,说明A是氢气,B是氯气。金属能与盐酸反应生成氢气,又因为C原子与B原子的电子层数相同,且最外层电子数之差为奇数,所以C是镁。原子最外层电子数为K层电子数的3倍的元素可以是O或S,因为单质为淡黄色固体的是硫,所以D是S。
(1)A:H B:Cl C:Mg D:S (2)Cl S
(3)H2O Cl2O7 MgO SO3

练习册系列答案
 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案
相关题目