题目内容
【题目】某100mL混合溶液中,H2SO4和HNO3的物质的量浓度分别是4.0mol/L和2.0mol/L,向该混合溶液中加入25.6g铜粉,加热,待充分反应后,静置,得到蓝色澄清溶液(假设反应后溶液体积不变)。下列说法中正确的是( )
A.产生的NO在标准状况下的体积是1.12L
B.反应后溶液中Cu2+的物质的量浓度为3.0mol/L
C.反应后溶液中H+的物质的量浓度为8.0mol/L
D.在反应后的溶液中加0.6molNaOH刚好使Cu2+完全沉淀
【答案】B
【解析】
![]() ,
,![]() ,
,![]() ,则该反应的离子反应方程式为:
,则该反应的离子反应方程式为:![]() ,于是得出:
,于是得出: ,显然
,显然![]() 的物质的量不足,则按
的物质的量不足,则按![]() 的物质的量进行计算;
的物质的量进行计算;
A. 产生的0.2mol NO,在标准状况下的体积是4.48L,A错误;
B. 反应后溶液中Cu2+的物质的量浓度为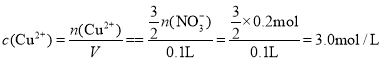 ,B正确;
,B正确;
C. 反应后溶液中H+有剩余,则![]() ,C错误;
,C错误;
D. 在反应后的溶液中有剩余的0.2mol H+,生成的0.3mol Cu2,加0.8molNaOH刚好在中和的基础上使Cu2+完全沉淀,D错误;
答案选B。

练习册系列答案
 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案
相关题目