题目内容
下列有关物质的性质和该性质的应用均正确的是( )
| A.常温下浓硫酸能使铝发生钝化,故可在常温下用铝制容器贮藏运输浓硫酸 |
| B.二氧化硅不与任何酸反应,可用石英制造耐酸容器 |
| C.二氧化氯具有还原性,可用于自来水的杀菌消毒 |
| D.铜的金属活泼性比铁的差,可在海轮外壳上装若干铜块以减缓其腐蚀 |
A
解析试题分析:铝制品在浓硫酸中发生钝化,能用铝制品储藏运输浓硫酸,A正确;二氧化硅可以和HF酸反应,B错误;ClO2 用于自来水消毒利用的是它的氧化性,C错误;用牺牲阳极的阴极保护法应该在轮船上镀上比铁更活泼的金属,如锌,D错误;故选A。
考点:本题考查的化合物性质及其应用。

练习册系列答案
相关题目
下列有关物质性质的应用正确的是
| A.氯化钠溶液显中性,可用铝制容器贮存氯化钠溶液 |
| B.碳酸钠溶液显碱性,可用热的纯碱溶液除去金属器件表面油污 |
| C.氮气化学性质通常不活泼,可将炽热的镁粉可放在氮气中冷却 |
| D.铜的金属性比铁弱,可将海轮浸水部分镶上铜锭以减缓船体腐蚀 |
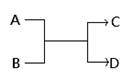
下表各组物质中,物质之间不可能实现如图所示转化的是
| 选项 | X | Y | Z | M |
| A | NH3 | NO | NO2 | O2 |
| B | Cl2 | FeCl3 | FeCl2 | Fe |
| C | Al | Al(OH)3 | NaAlO2 | NaOH |
| D | NaOH | Na2CO3 | NaHCO3 | CO2 |
(4分)(2012?广东)下列陈述Ⅰ、Ⅱ正确并且有因果关系的是( )
| 选项 | 陈述Ⅰ | 陈述Ⅱ |
| A | SO2有漂白性 | SO2可使溴水褪色 |
| B | SiO2有导电性 | SiO2可用于制备光导纤维 |
| C | 浓硫酸有强氧化性 | 浓硫酸可用于干燥H2和CO |
| D | Fe3+有氧化性 | FeCl3溶液可用于回收废旧电路板中的铜 |
A.A B.B C.C D.D
下列陈述Ⅰ、Ⅱ正确并且有因果关系的是( )
| 选项 | 陈述Ⅰ | 陈述Ⅱ |
| A | H2O2、SO2都能使酸性高锰酸钾褪色 | 前者表现出还原性后者表现出漂白性 |
| B | 纯银器表面在空气中渐渐变暗 | 发生了化学腐蚀 |
| C | SiO2能与氢氟酸及碱反应 | SiO2是两性氧化物 |
| D | BaSO4饱和溶液中加入饱和Na2CO3溶液有白色沉淀 | 说明Ksp(BaSO4)大于Ksp(BaCO3) |
下列推断正确的是
| | 事实 | 结论 |
| A | 常温下铁、铜均不溶于浓硫酸 | 常温下铁、铜与浓硫酸均不反应 |
| B | HCl与Na2CO3溶液反应生成CO2 | 可用饱和Na2CO3溶液除去CO2中的少量HCl |
| C | 氧化铜高温下生成红色物质,该物质可与稀硫酸反应 | 氧化铜高温下可分解生成Cu2O |
| D | 稀、浓硝酸分别与铜反应,还原产物分别为NO和NO2 | 稀硝酸氧化性比浓硝酸强 |