题目内容
下列有关工业生产的叙述正确的是
| A.合成氨生产中将NH3液化分离,可加快正反应速率,提高N2、H2的转化率 |
| B.联合制碱法是将二氧化碳和氨气通入饱和氯化钠溶液中,制得碳酸氢钠,再在高温下灼烧,转化为碳酸钠。 |
| C.硫酸工业中,在接触室安装热交换器是为了利用SO3转化为H2SO4时放出的热量 |
| D.电解饱和食盐水制烧碱采用离子交换膜法,可防止阴极室产生的C12进入阳极室 |
B
分析:A、减少生成物的浓度可以使化学平衡正向移动,使反应速率减慢;
B、根据联合制碱法的原理来分析;
C、硫酸工业中,SO3转化为H2SO4是在后面的吸收塔中进行的;
D、电解饱和食盐水制烧碱采用离子交换膜法,阳离子交换膜不允许阴离子通过,阴离子交换膜不允许阳离子通过.
解:A、合成氨生产中将NH3液化分离,提高N2、H2的转化率,但是会减慢反应速率,故A错误;
B、联合制碱法原是向氨化的饱和氯化钠溶液中通入足量的二氧化碳,使溶解度较小的碳酸氢钠从溶液中析出,其反应的化学方程式为:NaCl+CO2+NH3+H2O=NH4Cl+NaHCO3,故B正确;
C、硫酸工业中,在接触室安装热交换器是为了将放出的热量是用来预热没反应的二氧化硫与氧气的混合气体,SO3转化为H2SO4是在后面的吸收塔中进行的,故C错误;
D、电解饱和食盐水制烧碱采用离子交换膜法,可以防止阴极室产生的氢氧化钠、氢气和阳极室生成的Cl2混合,故D错误.
故选B.

练习册系列答案
相关题目

 压强
压强 的空气是为了________。
的空气是为了________。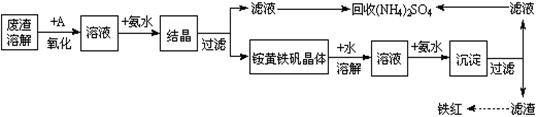
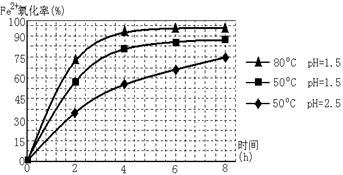
 量制备H2
量制备H2
 的流程图。写出下图中①②的化学式:① ,② ,吸收塔中发生的化学反应方程式为 。
的流程图。写出下图中①②的化学式:① ,② ,吸收塔中发生的化学反应方程式为 。
 4 SiHCl3(g)。达平衡后,H2与SiHCl3物质的量浓度分别为0.140mol/L和0.020mol/L,若H2全部来源于氯碱工业,理论上需消耗纯NaCl的
4 SiHCl3(g)。达平衡后,H2与SiHCl3物质的量浓度分别为0.140mol/L和0.020mol/L,若H2全部来源于氯碱工业,理论上需消耗纯NaCl的 质量为 kg。
质量为 kg。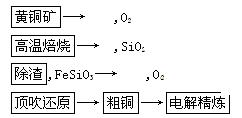
 到了NO和NO2的混合气体8.736L,与3.304LO2混合后,得到的混合气体恰好被水完全吸收。
到了NO和NO2的混合气体8.736L,与3.304LO2混合后,得到的混合气体恰好被水完全吸收。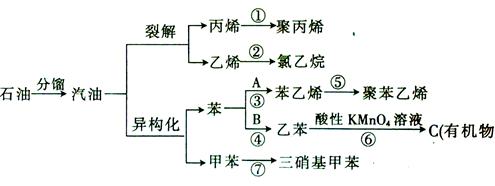
 ____________________________________________。
____________________________________________。