题目内容
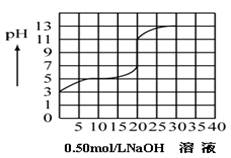
在100毫升某一元弱酸(Ka=10-3~10-7)的溶液中,以0.50mol/L氢氧化钠溶液滴定后得滴定曲线如下图所示,下列叙述正确的是:

| A.该弱酸在滴定前的浓度是0.15 mol/L: |
| B.该弱酸的电离常数(Ka)是10-5 |
| C.在滴定过程,为求滴定终点,最合适的指示剂是酚酞 |
| D.在滴定过程,为求滴定终点,最合适的指示剂是甲基橙 |
BC
可看出酸碱中和时所消耗的碱液的体积为20ml,设酸(假设为HA)的浓度为c mol/L,则0.1c=0.5×0.02,c=0.1mol/L,A不正确
原酸溶液pH=3,则:HA H++A+,H+及A+的浓度均为10-3 mol/L,由电离平衡常数:Ka=
H++A+,H+及A+的浓度均为10-3 mol/L,由电离平衡常数:Ka= ,B正确
,B正确
由于恰好中和时生成的是弱酸强碱盐溶液,呈碱性,最好找碱性条件下的变色的指示剂,也就是酚酞试剂,C正确,排除D
故答案为BC
原酸溶液pH=3,则:HA
 H++A+,H+及A+的浓度均为10-3 mol/L,由电离平衡常数:Ka=
H++A+,H+及A+的浓度均为10-3 mol/L,由电离平衡常数:Ka= ,B正确
,B正确由于恰好中和时生成的是弱酸强碱盐溶液,呈碱性,最好找碱性条件下的变色的指示剂,也就是酚酞试剂,C正确,排除D
故答案为BC

练习册系列答案
相关题目