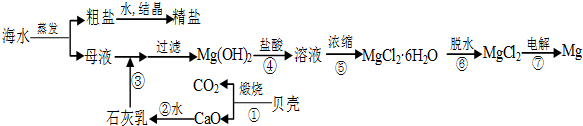
题目内容
在含有Mg(OH)2沉淀的饱和溶液中加入固体NH4Cl后,则Mg(OH)2沉淀( )
分析:氢氧化镁电离出来的OH-与NH4+结合生成弱电解质NH3?H2O,从而促进Mg(OH)2的溶解,据此分析解答.
解答:解:氢氧化镁溶液中存在溶解平衡Mg(OH)2?Mg 2++2OH-,Mg(OH)2电离出来的OH-与NH4+结合生成难电离的弱电解质NH3?H2O,氢氧根离子浓度降低,从而使Mg(OH)2的溶解平衡向右移动,促进氢氧化镁溶解,故Mg(OH)2能溶于NH4Cl溶液中,
故选A.
故选A.
点评:本题考查了难溶电解质的溶解平衡,从溶解平衡角度进行分析解答即可,难度不大.

练习册系列答案
相关题目