题目内容
在一定条件下,反应2A(g)+2B(g)![]() 3C(g)+D(g)达到平衡状态的标志是( )
3C(g)+D(g)达到平衡状态的标志是( )
A.单位时间内生成2n mol A,同时生成n mol D B.容器内压强不随时间而变化
C.单位时间内生成n mol B,同时消耗1.5n mol C D.容器内混合气体密度不随时间而变化
A
解析:
化学平衡的根本原因就是正、逆反应速率相等,反应混合物中各组分的百分含量保持不变;但必须明确:正逆反应在同时进行,单位时间内生成2n mol A,同时生成n mol D, A选项是正确的。C选项中单位的间内生成n mol B,同时消耗1.5n mol C,说明反应在逆向进行,不是平衡状态,C选项是错误的。对于B选项,因为本反应反应前后气体总体积不变,不论反应开始进行,还是达到平衡,体系的压强始终不变,B选项不能作为判定依据。对于D选项,本反应是一个气态反应,在恒容条件下,混合气体的密度无论起始还是达到平衡,始终不变,D选项不能作判定依据。

练习册系列答案
相关题目


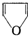 ,它的蒸气或者具有
,它的蒸气或者具有 结构的有机物的蒸气遇到用盐酸浸湿的松木片时发生显绿色的反应,叫做松片反应.
结构的有机物的蒸气遇到用盐酸浸湿的松木片时发生显绿色的反应,叫做松片反应. 互为同分异构体且具有松片反应的两种有机物的结构简式
互为同分异构体且具有松片反应的两种有机物的结构简式

 ,它用于塑料、清漆、医药和香烟香料.糠醛在NaOH溶液作用下发生自身氧化还原反应得到两种均含呋喃结构的有机物,它们的结构简式为
,它用于塑料、清漆、医药和香烟香料.糠醛在NaOH溶液作用下发生自身氧化还原反应得到两种均含呋喃结构的有机物,它们的结构简式为


