题目内容
(6分)某元素A,它的最高价氧化物的化学式是AO3,其气态氢化物里氢的质量分数为5.88%。已知A的原子核中质子数与中子数相等,则A的摩尔质量为 ,元素符号是 ,元素A位于第 周期 族,其最高价氧化物的水化物的化学式为 。
【答案】
32g·mol-1;S;3;ⅥA;H2SO4
【解析】元素A的最高价为+6价,故其最低负价为—2价,其氢化物的分子数为H2A;设A质量数为M,则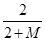 =5.88%,得出M=32,也就是A的摩尔质量为32g·mol-1;
=5.88%,得出M=32,也就是A的摩尔质量为32g·mol-1;
再由A的原子核中质子数与中子数相等知道它的质子数为16,为S元素,是第三周期第VIA族元素,最高价氧化物的水化物的化学式为H2SO4

练习册系列答案
相关题目
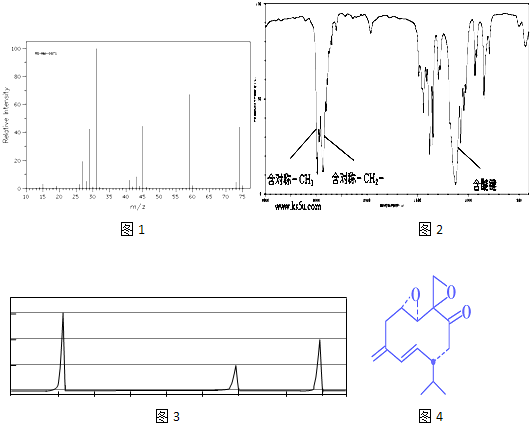

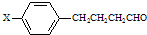 ,X可能的结构有
,X可能的结构有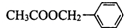 )是其中的一种,它可以从茉莉花中提取,也可以用甲苯和乙醇为原料进行人工合成.一种合成路线如:
)是其中的一种,它可以从茉莉花中提取,也可以用甲苯和乙醇为原料进行人工合成.一种合成路线如: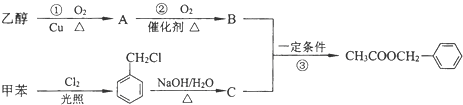

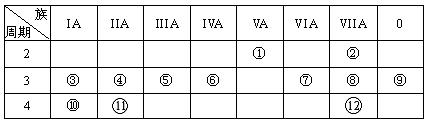
 温下⑦的单质和⑧的单质状态不同b.⑧的氢化物比⑦的氢化物稳定
温下⑦的单质和⑧的单质状态不同b.⑧的氢化物比⑦的氢化物稳定 原子半径最小的元素是 (填序号),它们可以形成 (填离子或共价)化合物,用电子式表示其形成过程如下: (2分)。
原子半径最小的元素是 (填序号),它们可以形成 (填离子或共价)化合物,用电子式表示其形成过程如下: (2分)。
