题目内容
下图为制取纯净干燥的Cl2并让其与铁发生反应的装置,A是Cl2发生装置,C、D为气体净化装置,E硬质玻璃管中装有细铁丝网;F为干燥的空广口瓶;烧杯G为尾气吸收装置。
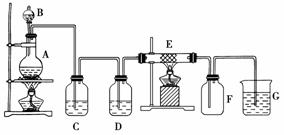
试回答:
(1)C、D、G三个装置所盛放的试剂分别是:
C_____________________________________________________
D___________
G
(2)F中的现象为___________________________,生成物是________。
(3)写出在A、E、G中发生反应的化学方程式为:
A: ;
E: ;
G
(1)C:饱和食盐水,D:浓硫酸,G:氢氧化钠溶液;
(2)产生棕黄色的烟,FeCl3 ;
(3)A MnO2 + 4HCl( 浓) MnCl2 + Cl2↑+ 2H2O
MnCl2 + Cl2↑+ 2H2O
E 2Fe + 3Cl2  2FeCl3
2FeCl3
G Cl2 + 2NaOH == NaCl + NaClO + H2O

 优百分课时互动系列答案
优百分课时互动系列答案环境监测测定水中溶解氧的方法是:①量取25mL水样,迅速加入固定剂MnSO4溶液和碱性KI溶液(含KOH),立即塞好瓶塞,反复振荡,使之充分反应,其反应式为: 2Mn2++O2+4OH-=2MnO(OH)2(该反应极快)②测定:开塞后迅速加入1mL~2mL浓硫酸(提供H+),使之生成I2,再用0.1000mol/L的Na2S2O3溶液滴定(以淀粉为指示剂),消耗V mL。有关反应式为:MnO(OH)2+2I-+4H+=Mn2++I2+3H2O ; I2+2S2O32-=2I-+S4O62-
| 滴定次数 | 待测液的体积/mL | 0.1000mol·L-1 Na2S2O3的体积/mL | ||
| 滴定前刻度 | 滴定后刻度 | 溶液体积/mL | ||
| 第一次 | 25.00 | 0.00 | 26.11 | 26.11 |
| 第二次 | 25.00 | 1.56 | 30.30 | 28.74 |
| 第三次 | 25.00 | 0.22 | 26.31 | 26.09 |
试回答:(1)消耗Na2S2O3的体积平均值为 ,水中溶解氧的量是(以g/L为单位,保留3位有效数字) 。
(2)滴定(I2和S2O32-反应)以淀粉为指示剂,终点时溶液 。
(3)判断下列操作引起的误差(填“偏大”、“偏小” “无影响”或“无法判断”)
①装标准液的滴定管读数:滴定前平视,滴定后俯视 ,
②未用标准液润洗滴定管____________,
③用固体配制Na2S2O3溶液时,其固体中含有对反应体系无影响的杂质____________,
④待测液的滴定管之前有气泡,取液后无气泡____________.
现有一瓶物质是甲和乙的混合物,已知甲和乙的某些性质如下表所示:
| 物质 | 熔点 | 沸点 | 密度 | 水中溶解性 |
| 甲 | -98 ℃ | 57.7 ℃ | 0.93 g·cm-3 | 可溶 |
| 乙 | -84 ℃ | 97 ℃ | 0.90 g·cm-3 | 可溶 |
据此,将甲和乙相互分离的最佳方法是( )
A.萃取法 B.过滤法 C.蒸馏法 D.分液法