题目内容
5.下列各组物质在一定条件下反应,不产生氧气的是( )| A. | Na2O2和H2O | B. | H2O2和MnO2 | C. | Na2O和H2O | D. | Na2O2和CO2 |
分析 根据物质之间的反应分析,Na2O2与CO2、H2O均能反应生成氧气,H2O2分解生成氧气,Na2O和H2O生成氢氧化钠.
解答 解:A.Na2O2和H2O反应生成氢氧化钠和氧气,反应中产生氧气,故A不选;
B.H2O2在二氧化锰催化作用下发生分解生成氧气,反应中产生氧气,故B不选;
C.Na2O和H2O发生化合反应生成NaOH,没有氧气生成,故C选;
D.Na2O2和CO2反应生成碳酸钠和氧气,反应中产生氧气,故D不选.
故选C.
点评 本题考查了元素化合物的性质,题目难度不大,侧重于考查了钠的化合物的性质,注意把握常见物质之间的反应.

练习册系列答案
相关题目
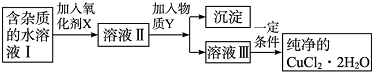
16.铁、铜单质及其化合物应用范围很广.现有含氯化亚铁杂质的氯化铜晶体(CuCl2•2H2O),为制取纯净的CuCl2•2H2O,首先将其制成水溶液,然后按如图步骤进行提纯:
已知Cu2+、Fe3+和Fe2+的氢氧化物开始沉淀和沉淀完全时的pH,见表:
(1)最适合作氧化剂X的是C.
A.K2Cr2O7 B.NaClO C.H2O2 D.KMnO4
(2)加入氧化剂的目的是将Fe2+氧化为Fe3+,便于生成沉淀而与Cu2+分离.
(3)加入的物质Y是CuO或Cu(OH)2或CuCO3或Cu2(OH)2CO3(写化学式),目的是调节溶液的pH.根据信息,溶液的pH范围应为调节溶液的pH至4~4.7.
(4)当c(Fe3+)=10-5mol/L时,认为沉淀完全,则Fe(OH)3的Ksp=1×10-35.
(5)结合方程式和必要文字说明解释不能将溶液Ⅲ直接蒸发结晶得到CuCl2•2H2O晶体的原因CuCl2+2H2O?Cu(OH)2+2HCl温度升高,HCl挥发,水解平衡正向移动,得到Cu(OH)2固体,而无法得到晶体.
(6)在饱和氯化铁溶液中加入碳酸钙粉末,发现碳酸钙逐渐溶解,同时还产生的现象有产生气泡和红褐色沉淀.

已知Cu2+、Fe3+和Fe2+的氢氧化物开始沉淀和沉淀完全时的pH,见表:
| Fe3+ | Fe2+ | Cu2+ | |
| 氢氧化物开始沉淀时的pH | 1.9 | 7.0 | 4.7 |
| 氢氧化物完全沉淀时的pH | 4 | 9.0 | 6.7 |
A.K2Cr2O7 B.NaClO C.H2O2 D.KMnO4
(2)加入氧化剂的目的是将Fe2+氧化为Fe3+,便于生成沉淀而与Cu2+分离.
(3)加入的物质Y是CuO或Cu(OH)2或CuCO3或Cu2(OH)2CO3(写化学式),目的是调节溶液的pH.根据信息,溶液的pH范围应为调节溶液的pH至4~4.7.
(4)当c(Fe3+)=10-5mol/L时,认为沉淀完全,则Fe(OH)3的Ksp=1×10-35.
(5)结合方程式和必要文字说明解释不能将溶液Ⅲ直接蒸发结晶得到CuCl2•2H2O晶体的原因CuCl2+2H2O?Cu(OH)2+2HCl温度升高,HCl挥发,水解平衡正向移动,得到Cu(OH)2固体,而无法得到晶体.
(6)在饱和氯化铁溶液中加入碳酸钙粉末,发现碳酸钙逐渐溶解,同时还产生的现象有产生气泡和红褐色沉淀.
13.室内空气污染的主要来源之一是人们现代生活所用的化工产品,如泡沫绝缘塑料制的办公桌、化纤地毯及书报、油漆等都会不同程度地释放出具有气味的气体,这种气体超标,也会引起人中毒,这种气体可能是( )
| A. | 二氧化碳 | B. | 甲醛 | C. | 氮气 | D. | 甲烷 |
20.下列反应的离子方程式中正确的是( )
| A. | Na2CO3溶液与Ba(OH)2溶液反应CO32-+Ba2+=BaCO3↓ | |
| B. | NaOH溶液与CH3COOH溶液反应H++OH-═H2O | |
| C. | NaHCO3溶液与盐酸反应CO32-+2H+=CO2↑+H2O | |
| D. | NaHCO3溶液与CaCl2溶液反应CO32-+Ca2+=CaCO3↓ |
10.下列说法错误的是( )
| A. | 对大型船舶的外壳进行的“牺牲阳极的阴极保护法”,是应用了原电池原理 | |
| B. | 电镀时,通常把待镀的金属制品作阴极,把镀层金属作阳极 | |
| C. | 对于冶炼像钠、钙、镁、铝等这样活泼的金属,电解法几乎是唯一可行的工业方法 | |
| D. | 氯化铝的熔点比氧化铝低,因此工业上最好采用电解熔融氯化铝来制备单质铝 |
17.下列叙述中,正确的是( )
| A. | 在氧化还原反应中,肯定有一种元素被氧化,另一种元素被还原 | |
| B. | 得电子越多的氧化剂,其氧化性就越强 | |
| C. | 阳离子只有氧化性,阴离子只有还原性 | |
| D. | 有单质参加的反应不一定属于氧化还原反应 |
