题目内容
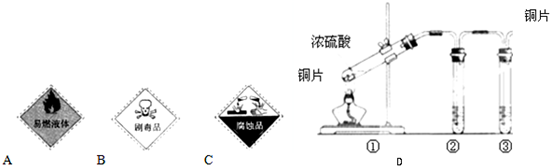
为研究盛装浓硫酸的铁质材料(碳素钢)与浓硫酸的反应,某学习小组进行了以下探究活动:
【实验】
取一铁钉放入一定体积浓硫酸中,加热,充分反应后得到溶液X并收集到气体Y.
①甲同学认为x中除Fe3+外还可能含有Fe2+.若要确认其中的Fe2+,应选用______(选填序号)
a.KSCN溶液和氯水b.铁粉和KSCN溶液c.浓氨水d.酸性:KMn04溶液
②为分析气体成分,乙同学取448mL(标准状况)气体Y通人足量溴水中,发生的反应式为:Br2+SO2+2H20═2HBr+H2S04,然后加入足量BaCl2溶液,经适当操作后得干燥固体2.33g
【提出猜想】
分析上述实验中SO2的体积分数的结果,同学们认为Y中还可能含有其它气体并作如下猜测:
猜想一:Y气体中可能含有H2;
猜想二:______
猜想三:______
【设计实验,验证猜想】
为验证以上猜想,同学们准备用下列如图装置设计探究实验(装置可重复使用,夹持仪器省略).
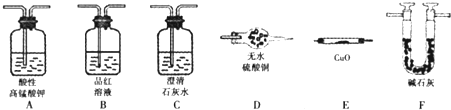
(1)实验装置连接次序为A→______→______→F______→______→F
(2)装置B中试剂作用是______.
(3)猜想一的理由是______(用化学方程式表示).
(4)如果猜想一成立,预计实验现象应该是______.
【实验】
取一铁钉放入一定体积浓硫酸中,加热,充分反应后得到溶液X并收集到气体Y.
①甲同学认为x中除Fe3+外还可能含有Fe2+.若要确认其中的Fe2+,应选用______(选填序号)
a.KSCN溶液和氯水b.铁粉和KSCN溶液c.浓氨水d.酸性:KMn04溶液
②为分析气体成分,乙同学取448mL(标准状况)气体Y通人足量溴水中,发生的反应式为:Br2+SO2+2H20═2HBr+H2S04,然后加入足量BaCl2溶液,经适当操作后得干燥固体2.33g
【提出猜想】
分析上述实验中SO2的体积分数的结果,同学们认为Y中还可能含有其它气体并作如下猜测:
猜想一:Y气体中可能含有H2;
猜想二:______
猜想三:______
【设计实验,验证猜想】
为验证以上猜想,同学们准备用下列如图装置设计探究实验(装置可重复使用,夹持仪器省略).

(1)实验装置连接次序为A→______→______→F______→______→F
(2)装置B中试剂作用是______.
(3)猜想一的理由是______(用化学方程式表示).
(4)如果猜想一成立,预计实验现象应该是______.
实验:①亚铁离子能使酸化的高锰酸钾褪色,溶液中已经有Fe3+,选择a会造成干扰,选b只能检验溶液中含有+3价铁离子,选c会造成两种沉淀,受氢氧化铁颜色的影响无法辨别,只能选d,
故答案为:d;
【提出猜想】碳素钢中含有碳元素,碳能够与浓硫酸在加热条件下反应生成二氧化碳,所以混合气体中可能含有二氧化碳气体;铁和浓硫酸反应生成二氧化硫,随反应进行硫酸浓度减小变为稀硫酸后铁和稀硫酸反应生成氢气,所以可能情况有如下三种:猜想一:Y气体中可能含有H2;猜想二:Y气体中可能含有CO2;猜想三:Y气体中可能含有H2和CO2 ,
故答案为:Y气体中可能含有CO2;Y气体中可能含有H2和CO2 ;
(1)碳素钢中含有碳元素,推断所的气体中可能含有二氧化碳,结合图中设计装置的目的,可知检验二氧化碳的方法是首先将二氧化硫除去→确认二氧化硫已经完全除去→澄清石灰水,对于氢气的检验则可通过与灼热氧化铜的反应现象和对产物水的验证来实现,验证气体存在的顺序为:SO2→CO2→CO和H2被氧化→H2O→CO2,实验中要避免其它物质的性质干扰,即为A→B→C→F→E→D,
故答案为:B;C;E;D;
(2)CO2气体和SO2气体都能使澄清石灰水变浑浊,检验CO2气体的存在应先除去SO2气体并检验是否除尽,
故答案为:检验SO2是否除尽;
(3)气体中如含有H2,发生的反应为Fe+H2SO4═FeSO4+H2↑,
故答案为:Fe+H2SO4═FeSO4+H2↑;
(4)含有H2,与CuO在加热条件下反应生成铜和水,E中固体由黑色氧化铜生成红色铜,D中无色硫酸铜吸水生成五水硫酸铜蓝色晶体,
故答案为:E中固体由黑变红,D中固体由白变蓝色.
故答案为:d;
【提出猜想】碳素钢中含有碳元素,碳能够与浓硫酸在加热条件下反应生成二氧化碳,所以混合气体中可能含有二氧化碳气体;铁和浓硫酸反应生成二氧化硫,随反应进行硫酸浓度减小变为稀硫酸后铁和稀硫酸反应生成氢气,所以可能情况有如下三种:猜想一:Y气体中可能含有H2;猜想二:Y气体中可能含有CO2;猜想三:Y气体中可能含有H2和CO2 ,
故答案为:Y气体中可能含有CO2;Y气体中可能含有H2和CO2 ;
(1)碳素钢中含有碳元素,推断所的气体中可能含有二氧化碳,结合图中设计装置的目的,可知检验二氧化碳的方法是首先将二氧化硫除去→确认二氧化硫已经完全除去→澄清石灰水,对于氢气的检验则可通过与灼热氧化铜的反应现象和对产物水的验证来实现,验证气体存在的顺序为:SO2→CO2→CO和H2被氧化→H2O→CO2,实验中要避免其它物质的性质干扰,即为A→B→C→F→E→D,
故答案为:B;C;E;D;
(2)CO2气体和SO2气体都能使澄清石灰水变浑浊,检验CO2气体的存在应先除去SO2气体并检验是否除尽,
故答案为:检验SO2是否除尽;
(3)气体中如含有H2,发生的反应为Fe+H2SO4═FeSO4+H2↑,
故答案为:Fe+H2SO4═FeSO4+H2↑;
(4)含有H2,与CuO在加热条件下反应生成铜和水,E中固体由黑色氧化铜生成红色铜,D中无色硫酸铜吸水生成五水硫酸铜蓝色晶体,
故答案为:E中固体由黑变红,D中固体由白变蓝色.

练习册系列答案
 名师指导期末冲刺卷系列答案
名师指导期末冲刺卷系列答案
相关题目