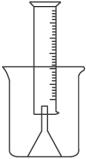
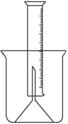
题目内容
(14分)测定一定质量的铝锌合金与强酸溶液反应产生的氢气的体积,可以求得合金中铝和锌的质量分数及物质的量分数。现有下列实验用品:中学化学实验常用仪器、1000 mL烧杯、100 mL量筒、短颈玻璃漏斗、铜网、铝锌合金样品、浓盐酸(密度1.19 g·cm-3)、水。按图示装置进行实验,回答下列问题。(设合金样品完全反应,产生的气体体积不超过100 mL)
(1).补充下列实验步骤,直到反应开始进行(铁架台和铁夹的安装可省略):
①将称量后的合金样品用铜网小心包裹好,放在1000 mL烧杯底部,把短颈漏斗倒扣在样品上面。
②_________________________________________________________________________。
③_________________________________________________________________________。
④_________________________________________________________________________。
(2).合金样品用铜网包裹的目的是什么?
________________________________________________________________________。
(3).已知一定质量的铝锌合金的总物质的量为n,实验测得的气体体积为V1mL(已经换算为标准状况)。则铝锌合金中铝的物质的量分数为:_________________。(用含n和V1的式子表示)
(4)本装置也可用于测定金属锌(或其它金属)的相对原子质量,若m g金属锌进行实验,测得的气体体积为V2mL(已经换算为标准状况)。则金属锌的相对原子质量为:_________________。(用含m和V2的式子表示)
(1)氢气用向下排空气法或排水法收集,又因为需要测量氢气的体积,所以要借助于量筒。正确的步骤是:②往烧杯中加水直至水浸没漏斗颈。③在100ml量筒中装满水,倒置在盛水的烧杯中(量筒中不应留有气泡),使漏斗颈插入量筒中,烧杯中水面到杯口至少保留约100ml空间。④将长颈漏斗(玻璃棒)插入烧杯并接近烧杯底部,通过条慢慢加入浓盐酸,至有气体产生。
(2)使样品在反应时能保持在烧杯底部适当位置(或避免反应时样品漂浮)。
解析:(1)氢气用向下排空气法或排水法收集,又因为需要测量氢气的体积,所以要借助于量筒。正确的步骤是:②往烧杯中加水直至水浸没漏斗颈。③在100ml量筒中装满水,倒置在盛水的烧杯中(量筒中不应留有气泡),使漏斗颈插入量筒中,烧杯中水面到杯口至少保留约100ml空间。④将长颈漏斗(玻璃棒)插入烧杯并接近烧杯底部,通过条慢慢加入浓盐酸,至有气体产生。
(2)反应中生成的氢气溶液使固体漂浮,所以用铜网包裹使其固定在底部。
(3)、(4)根据应该反应的方程式可列式进行计算或根据得失电子守恒进行计算。

 测定一定质量的铝锌合金与强酸溶液反应产生的氢气的体积,可以求得合金中铝和锌的质量分数.现有下列实验用品:中学化学实验常用仪器.800毫升烧杯.100毫升量筒.短颈玻璃漏斗.铜网.铝锌合金样品.浓盐酸(密度1.19克/毫升).水.按图示装置进行实验,回答下列问题.(设合金样品完全反应,产生的气体体积不超过100毫升)
测定一定质量的铝锌合金与强酸溶液反应产生的氢气的体积,可以求得合金中铝和锌的质量分数.现有下列实验用品:中学化学实验常用仪器.800毫升烧杯.100毫升量筒.短颈玻璃漏斗.铜网.铝锌合金样品.浓盐酸(密度1.19克/毫升).水.按图示装置进行实验,回答下列问题.(设合金样品完全反应,产生的气体体积不超过100毫升)