题目内容
原子结构决定元素的性质,下列说法中,正确的是
| A.Na、Al、Cl的原子半径依次减小,Na+、Al3+、Cl-的离子半径也依次减小 |
| B.在第ⅥA族元素的氢化物(H2R)中,热稳定性最强的其沸点也一定最高 |
| C.第2周期元素的最高正化合价都等于其原子的最外层电子数 |
| D.非金属元素的非金属性越强,其氧化物对应水化物的酸性也一定越强 |
B
解析试题分析:A、Na+、Al3+为10e?离子,Cl?为18e?离子,Cl?半径大于Na+、Al3+半径,错误;B、因为F元素的非金属性最强,所以在第ⅥA族元素的氢化物(H2R)中,HF热稳定性最强,因为HF分子间能形成氢键,所以HF的沸点也最高,错误;C、第2周期元素非金属性强的O元素、F元素没有最高正化合价,错误;D、非金属元素的非金属性越强,其最高价氧化物对应水化物的酸性也一定越强,错误。
考点:本题考查元素周期律。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列各组原子中,彼此化学性质一定相似的是
| A.原子核外电子排布式为1s2的X原子与原子核外电子排布式为1s22s2的Y原子 |
| B.原子核外M层上仅有两个电子的X原子与原子核外N层上仅有两个电子的Y原子 |
| C.2p轨道上有三个未成对电子的X原子与3p轨道上有三个未成对电子的Y原子 |
| D.最外层都只有一个电子的X、Y原子 |
下列说法中错误的是( )。
| A.质子数相同的原子,其核外电子排布也相同 |
| B.质量数相同的不同原子,其化学性质一定相同 |
| C.金属性越强,其原子在反应中越易得到电子 |
| D.非金属性越强,其阴离子越难失去电子 |
下列各组比较中正确的是( )。
| A.锂与水反应不如钠与水反应剧烈 |
| B.还原性:K>Na>Li,故K可以从NaCl溶液中置换出金属钠 |
| C.密度:Li<Na<K<Rb<Cs |
| D.碱性:LiOH>NaOH>KOH |
下列有关表述正确的是( )
| A.硫离子的电子排布式:1s22s22p63s23p4 |
B.H2O的电子式: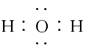 |
C.N原子最外层电子的轨道表示式: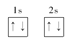 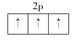 |
D.K的原子结构示意图: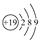 |
主族元素在周期表中的位置取决于该元素原子的( )。
| A.相对原子质量和核外电子数 |
| B.电子层数和最外层电子数 |
| C.相对原子质量和最外层电子数 |
| D.电子层数和次外层电子数 |
A和B是短周期元素,A2-与B+的核外电子总数之差为8,则下列说法正确的是( )
| A.A和B的原子序数之差为8 |
| B.A和B原子的最外层电子数之和为8 |
| C.A和B原子的最外层电子数之差为7 |
| D.A和B原子的核外电子数总和可能为11 |