题目内容
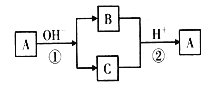
【题目】如图所示,某同学设计了一个甲醚(CH3OCH3)燃料电池并探究氯碱工业原理和原理和粗铜的精炼原理,乙装置中X为阳离子交换膜。根据要求回答下列相关问题:
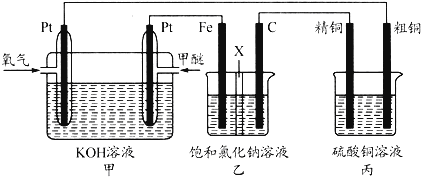
(1)通入氧气的电极为_____(填“正极”或“负极”),写出负极的电极反应式_____.
(2)铁电极为_____(填“阳极”或“阴极”),石墨电极的电极反应式为_____.
(3)反应一段时间后,乙装置中生成NaOH主要在_____(填“铁极”或“石墨极”)区.
(4)如果粗铜中含有锌、银等杂质,丙装置中阳极上电极反应式为_____,反应一段时间,硫酸铜溶液浓度将_____(填“增大”“减小”或“不变”).
(5)若在标准状况下,有2.24L氧气参加反应,则乙装置中铁电极上生成的气体在标准状况下的体积为_____;丙装置中阴极析出铜的质量为_____.
【答案】 正极 CH3OCH3-12e-+16OH-=2CO32-+11H2O 阴极 2Cl--2e-═Cl2↑ 铁极 Zn-2e-=Zn2+、Cu-2e-=Cu2+ 减小 4.48L 12.8 g.
【解析】(1)燃料电池中,通入燃料的电极是负极,通入氧化剂的电极是正极,所以通入氧气的电极是正极;碱性电解质溶液,负极上甲醚失电子和氢氧根离子反应生成碳酸根离子和水,故电极反应式为:CH3OCH3-12e-+16OH-=2CO32-+11H2O。
(2)乙池属于电解池,铁电极连接燃料电池的负极,所以是阴极,石墨电极是阳极,在阳极上氯离子失电子生成氯气,电极反应式为:2Cl--2e-=Cl2↑。
(3)乙池中阳极是碳,阴极是铁,阳极上氯离子失电子生成氯气,阴极上氢离子得电子生成氢气,使阴极附近氢氧根离子浓度大于氢离子浓度溶液而呈碱性,所以乙装置中生成氢氧化钠主要在阴极区,即铁极区。
(4)丙装置如果粗铜中含有锌、银等杂质,锌比铜还原性更强,所以阳极上锌和铜放电,电极反应式为Zn-2e-=Zn2+、Cu-2e-=Cu2+;阴极上析出铜单质,根据得失电子数相等,阳极上溶解的铜小于阴极上析出的铜,所以反应一段时间后,丙装置中硫酸铜溶液浓度将减小。
(5)根据串联电路中转移电子数相等可得关系式:O2~2H2~2Cu~4e-,标准状况下,2.24L氧气是0.1mol,所以铁电极上生成H2是0.2mol,在标准状况下的体积为4.48L;丙装置中阴极析出铜0.2mol,质量为12.8g。

 通城学典默写能手系列答案
通城学典默写能手系列答案