题目内容
(14分) HNO2是一种弱酸,且不稳定,易分解生成NO和NO2;它能被常见的强氧化剂氧化;在酸性溶液中它也是一种氧化剂,如能把Fe2+氧化成Fe3+。AgNO2是一种难溶于水、易溶于酸的化合物。试回答下列问题:
(1)人体正常的血红蛋白含有Fe2+。若误食亚硝酸盐(如NaNO2),则导致血红蛋白中的
Fe2+转化为Fe3+而中毒,服用维生素C可解毒。下列叙述不正确的是________(填序号)。
A.亚硝酸盐被还原 B.维生素C是还原剂
C.维生素C将Fe3+还原为Fe2+ D.亚硝酸盐是还原剂
(2)下列方法中,不能用来区分NaNO2和NaCl的是________(填序号)。
A.测定这两种溶液的pH
B.分别在两种溶液中滴加甲基橙
C.在酸性条件下加入KI—淀粉溶液来区别
D. 用AgNO3和HNO3两种试剂来区别
(3)某同学把新制的氯水加到NaNO2溶液中,观察到氯水褪色,同时生成NaNO3和HCl,请写出反应的离子方程式:___________________________________。
(4) Fe与过量稀硫酸反应可以制取FeSO4。若用反应所得的酸性溶液,将Fe2+转化为
Fe3+,要求产物纯净,可选用的最佳试剂是________(填序号)。
a.Cl2 b.Fe c.H2O2 d.HNO3
(5)若FeSO4和O2的化学计量数比为2∶1,试配平下列方程式:
FeSO4+K2O2―→K2FeO4+K2O+K2SO4+O2↑
(6)高铁酸钾(K2FeO4)是一种新型、高效的绿色水处理剂,在水中发生反应生成氢氧化铁胶体。高铁酸钾作为水处理剂发挥的作用是________________________________。
(1)D(2分) (2)B(2分)(3)NO+Cl2+H2O===NO+2H++2Cl-(3分)
(4)c(2分) (5) 2 6 2 2 2 1(3分) (6)净水、消毒(2分)
【解析】(1)亚硝酸银能把亚铁离子转化为铁离子,说明亚硝酸银具有氧化性。服用维生素C可解毒,这说明维生素能把铁离子还原为亚铁离子,因此选项D是错误的,答案选D。
(2)亚硝酸钠水解显碱性,氯化钠不水解显中性,A正确。甲基橙的变色范围是3.1~4.4,所以,选项B中溶液都是显黄色的,无法鉴别,B不正确。亚硝酸钠具有氧化性,能把碘化钾氧化生成单质碘,碘遇淀粉显蓝色,C正确,氯化钠和硝酸银反应生成白色沉淀,D正确,答案选B。
(3)氯水褪色,说明氯气倍还原,作氧化剂,根据生成物可知,方程式为NO+Cl2+H2O===NO+2H++2Cl-。
(4)铁没有氧化性,b不正确。氯气、双氧水的还原产物分别是氯离子、水,所以c正确,a不正确。D中会引起NO3-,所以d也不正确。答案选c。
(5)铁的化合价从+2价,升高到+6价,失去4个电子,根据反应中转移8个电子。氧气是氧化产物,又转移2个电子,所以反应中共失去10个电子。所以根据电子的得失守恒可知,硫酸亚铁和过氧化钾的物质的量之比是2︰6,然后通过观察法配平其它的。
(6)高铁酸钾中铁的化合价是+6价,具有强氧化性,能起杀毒作用。生成物铁离子水解,生成氢氧化铁胶体能吸附水中的悬浮物,起净水作用,所以高铁酸钾的作用是净水、消毒。

 每课必练系列答案
每课必练系列答案 巧学巧练系列答案
巧学巧练系列答案
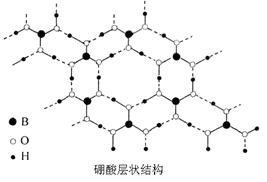
 [B(OH)4]-+H+,写出硼酸与NaOH溶液反应的离子方程式_______________________________________________。
[B(OH)4]-+H+,写出硼酸与NaOH溶液反应的离子方程式_______________________________________________。