题目内容
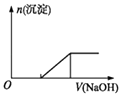
【题目】向四只盛有一定量NaOH溶液的烧杯中通入不同的CO2气体,再在所得溶液中逐滴加入稀盐酸至过量,并将溶液加热,产生的CO2气体与HCl物质的量的关系如图:(忽略CO2的溶解和HCl的挥发) 
则下列分析都正确的组合是( )
①Ⅰ图对应溶液中的溶质为NaHCO3
②Ⅱ图对应溶液中的溶质为Na2CO3和NaHCO3 , 且二者的物质的量之比为1:1
③Ⅲ图对应溶液中的溶质为NaOH和NaHCO3 , 且二者的物质的量之比为1:1
④Ⅳ图对应溶液中的溶质为Na2CO3 .
A.①②
B.①③
C.②④
D.②③
【答案】A
【解析】解:向一定量NaOH溶液的烧杯中通入不同量的CO2气体,当二氧化碳少量时,产物是NaOH和Na2CO3的混合物,当NaOH和CO2恰好完全反应时,产物只有Na2CO3 , 当二氧化碳过量时,产物可能只有NaHCO3 , 也可能是Na2CO3和NaHCO3的混合物.Ⅰ、图中刚开始加入HCl就产生了二氧化碳,因此溶质只能是NaHCO3 , 故①正确;
Ⅱ、从图中看出刚滴下去盐酸一个单位后产生了二氧化碳,说明此时碳酸根的量是一个单位(盐多酸少,碳酸钠和盐酸一比一反应生成碳酸氢钠),后来盐酸加了两个单位才把所有二氧化碳反应出来,说明溶液中总的碳酸氢根量为两个单位,但有一个单位的是之前碳酸根得来的,所以原溶液中碳酸根的量和碳酸氢根的量相等,即c(Na2CO3)=c(NaHCO3),故②正确;
Ⅲ、从图中看出,滴入了两个单位的盐酸后才开始产生气泡,且产生二氧化碳所消耗的盐酸也是两个单位,说明产物只有Na2CO3 , 物料守恒可知:c(Na+)=2c(CO32﹣)+2c(HCO3﹣)+2c(H2CO3);故③错误;
Ⅳ、从图中看出,滴入了两个单位的盐酸后才开始产生气泡,说明产物是NaOH和Na2CO3的混合物,一个单位的盐酸和NaOH反应,第二个单位的盐酸和Na2CO3反应生成NaHCO3 , 后由图中可看出,NaHCO3又消耗了一个单位的盐酸,则含有氢氧化钠和碳酸钠的量之比是1:1,故④错误.
由上分析知①②正确,③④错误,
故选:A.

 阅读快车系列答案
阅读快车系列答案【题目】下列物质的化学性质与实际应用对应关系正确的是( )
化学性质 | 实际应用 | |
A | NH3具有碱性 | 用作制冷剂 |
B | SO2是酸性氧化物 | 用于纸张漂白 |
C | 漂白粉具有氧化性 | 用于漂白织物 |
D | FeCl3能与碱溶液反应 | 用于蚀刻铜制线路板 |
A.AB.BC.CD.D
【题目】A~E是核电荷数均小于20的元素,其结构或性质信息如下表
元素 | A | B | C | D | E |
性质或结构信息 | 其原子核内只有1个质子 | 其单质在空气中体积含量最多 | 其原子M层有3个电子 | 食盐中的金属元素 | 单质在常温、常压下是黄绿色的气体 |
请根据表中的信息回答下列问题:
(1)D离子的结构示意图: , B原子的电子式: , E离子的电子式: .
(2)和B元素的氢化物所含电子数相同的分子有多种,写出任意2种: , .
(3)A元素与E元素组成的化合物的电离方程式: .
(4)如图所示为元素周期表中钾元素框图,数据“39.10”表示的是;写出钾离子的电子式: .