题目内容
(10分)Ⅰ.已知NaHS04是一种酸式盐,在工业上应用广泛,根据NaHS04的性质回答下列问题:
(1)写出NaHS04在水溶液中的电离方程式:
(2)若向NaHS04溶液中滴加Ba(OH)2至SO42-完全沉淀时的离子方程式为
(3)滴加Ba(0H)2溶液使溶液呈中性时的化学方程式为
Ⅱ.(4)若在标准状况下,将V L HCl气体溶于lL水中,所得溶液密度为dg/ml,则此溶液的物质的量浓度为
(5) 一定质量的铝铁合金溶于足量的NaOH溶液中,完全反应后产生3.36 L(标准状况下)气体;用同样质量的铝铁合金完全溶于足量的盐酸中,在标准状况下产生5.6 L(标准状况下)的气体,则该合金中铝、铁的物质的量之比为
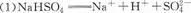
(2)
(3)2NaHSO4+Ba(OH)2=Na2SO4+BaSO4+2H2O
(4)1000d/(36.5v+22400)
(5)1:1
解析试题分析:Ⅰ.依据各类方程式书写的要求和题意要求书写,注意电荷守恒和方式式配平。
Ⅱ.(4)溶液的浓度可用质量分数和物质的量浓度两种不同的物理量来表示。溶液的质量为 ,溶液的体积为
,溶液的体积为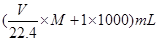 。则物质的量浓度为
。则物质的量浓度为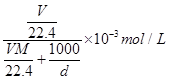 ,化简即得
,化简即得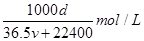 。
。
(5)将铝铁合金溶于NaOH溶液中时,只有铝参与反应,而铁不反应,此时生成的3.36 L(即0.15 mol)氢气是由反应2Al+2NaOH+2H2O===2NaAlO2+3H2↑生成的,故合金中n(Al)=0.15 mol×=0.1 mol;当同样质量的合金与盐酸反应时,铝参与反应生成的H2为0.15 mol,则由Fe置换出的n(H2)=0.25 mol-0.15 mol=0.1 mol,即合金中含Fe的物质的量也为0.1 mol
考点:各类方程式的书写;化学计量的计算
点评:本题主要考查电离方程式、离子方程式、化学方程式的书写和化学计算,综合性较强,题目难度较大。

(共10分)已知某有机物中n(C): n(H)=1, 将W1g该有机物在足量氧气中充分燃烧,消耗标准状况下的氧气V L,产物只有CO2和H2O,且m(CO2)=w2g,m(H2O)=W3g。
(1)若通过计算来确定该有机物是否含氧,除已知的碳氢原子个数比外,还至少需上述数据中的 个,这几个数据的组合共有 种,将这些组合一一填入下列空格中。
说明:①选用V、W1、W2、W3表示,不必列出具体计算式;
②每个空格中填一种组合,有几种组合就填几种,不必填满。
|
|
|
|
|
|
|
|
|
|
(2)当W1与V之间满足 条件时,该有机物中一定没有氧原子,当W1与V之间满足 条件时,该有机物中一定含有氧原子。
(3)W1g有机物中含氧的质量为 g。(用含W1、W2的代数式表示)
(共10分)已知某有机物中n(C): n(H)="1," 将W1g该有机物在足量氧气中充分燃烧,消耗标准状况下的氧气V L,产物只有CO2和H2O,且m(CO2)=w2g,m(H2O)=W3g。
(1)若通过计算来确定该有机物是否含氧,除已知的碳氢原子个数比外,还至少需上述数据中的 个,这几个数据的组合共有 种,将这些组合一一填入下列空格中。
说明:①选用V、W1、W2、W3表示,不必列出具体计算式;
②每个空格中填一种组合,有几种组合就填几种,不必填满。
| | | | |
| | | | |
(3)W1g有机物中含氧的质量为 g。(用含W1、W2的代数式表示)
(共10分)已知某有机物中n(C): n(H)=1, 将W1g该有机物在足量氧气中充分燃烧,消耗标准状况下的氧气V L,产物只有CO2和H2O,且m(CO2)=w2g,m(H2O)=W3g。
(1)若通过计算来确定该有机物是否含氧,除已知的碳氢原子个数比外,还至少需上述数据中的 个,这几个数据的组合共有 种,将这些组合一一填入下列空格中。
说明:①选用V、W1、W2、W3表示,不必列出具体计算式;
②每个空格中填一种组合,有几种组合就填几种,不必填满。
|
|
|
|
|
|
|
|
|
|
(2)当W1与V之间满足 条件时,该有机物中一定没有氧原子,当W1与V之间满足 条件时,该有机物中一定含有氧原子。
(3)W1g有机物中含氧的质量为 g。(用含W1、W2的代数式表示)
(共10分)已知某有机物中n(C): n(H)=1, 将W1g该有机物在足量氧气中充分燃烧,消耗标准状况下的氧气V L,产物只有CO2和H2O,且m(CO2)=w2g,m(H2O)=W3g。
(1)若通过计算来确定该有机物是否含氧,除已知的碳氢原子个数比外,还至少需上述数据中的 个,这几个数据的组合共有 种,将这些组合一一填入下列空格中。
说明:①选用V、W1、W2、W3表示,不必列出具体计算式;
②每个空格中填一种组合,有几种组合就填几种,不必填满。
(2)当W1与V之间满足 条件时,该有机物中一定没有氧原子,当W1与V之间满足 条件时,该有机物中一定含有氧原子。
(3)W1g有机物中含氧的质量为 g。(用含W1、W2的代数式表示)