题目内容
18.20mL由两种气态烃组成的混合物,和足量的O2完全燃烧生成了50mL H2O(g)和40mL CO2 (气体体积均在同温同压下测定).该混合物的组成和体积比正确的是( )| A. | C2H4、C2H6(3:1) | B. | CH4、C3H6 (1:1) | C. | C2H2、C2H4(3:2) | D. | C2H6、C3H8(1:2) |
分析 20mL由两种气态烃组成的混合物,和足量的O2完全燃烧生成了50mL H2O(g)和40mL CO2 (气体体积均在同温同压下测定),根据相同条件下气体的体积之比等于物质的量之比计算出混合气态烃的平均分子式,然后对各选项进行判断.
解答 解:相同条件下气体的体积之比等于物质的量之比,则混合烃与生成水、二氧化碳的物质的量之比为:20mL:50mL:40mL=2:5:4,
该混合烃中平均C、H原子数分别为:N(C)=$\frac{4×1}{2}$=2、N(H)=$\frac{5×2}{2}$=5,
所以该混合烃的平均分子式为:C2H5,
A.C2H4、C2H6按照体积比3:1时平均H原子数为:$\frac{4×3+6×1}{3+1}$=4.5≠5,故A错误;
B.CH4、C3H6 按照体积比1:1混合时的平均分子式为C2H5,符合条件,故B正确;
C.C2H2、C2H4的分子中含有H原子数都小于5,则平均H原子数一定不可能为5,故C错误;
D.C2H6、C3H8分子中含有的H原子数都大于5,其平均H原子数不可能为5,故D错误;
故选B.
点评 本题考查了混合物反应的计算,题目难度中等,明确平均分子式中有机物计算中的应用方法为解答关键,试题侧重考查学生的分析能力及灵活应用能力.

练习册系列答案
 名师金手指领衔课时系列答案
名师金手指领衔课时系列答案
相关题目
8.水是一种极弱的电解质,在室温下水的电离常数为1.8×10-16,若平均每n个水分子只有一个水分子能电离,则n是( )
| A. | 1×10-4 | B. | 55.6×107 | C. | 1×107 | D. | 6.02×1021 |
6.下列关于苯的叙述中,正确的是( )
| A. | 苯在一定条件下能与浓硝酸发生加成反应生成硝基苯 | |
| B. | 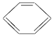 表示苯的分子结构,其中含有碳碳单键和碳碳双键,因此苯的性质跟乙烯的相似 表示苯的分子结构,其中含有碳碳单键和碳碳双键,因此苯的性质跟乙烯的相似 | |
| C. | 苯的分子式为C6H6,分子中氢原子个数比较少,能和溴水反应 | |
| D. | 苯分子的碳环为平面正六边形结构,6个碳原子之间的键完全相同 |
3.下列操作方法不正确的是( )
| A. | 用酒精清洗沾在皮肤上的少量苯酚 | B. | 用灼烧的方法检验羊毛线和棉线 | ||
| C. | 银镜反应后的试管用稀硝酸清洗 | D. | 用分液漏斗分离苯和甲苯 |
7.在一定温度下,可逆反应A2(g)+B2(g)?2AB(g)达到平衡的标志是( )
| A. | A2、B2、AB的浓度相等 | |
| B. | 容器中的压强不再随时间变化而变化 | |
| C. | A2、B2、AB的浓度之比为1:1:2 | |
| D. | 单位时间内生成n mol A2的同时生成2n molAB |
8.下列有关实验原理、装置、操作或结论的描述中,正确的是( )

| A | 用图①装置蒸发稀盐酸制浓盐酸 |
| B | 用图②装置分液时,下层液体从分液漏斗下口放出,关闭活塞再将上层液体从上口倒出 |
| C | 用图③洗涤沉淀时,漏斗中加入适量蒸馏水,搅拌并滤干 |
| D | 用图④装置,分离四氯化碳与苯的混合溶液 |

| A. | A | B. | B | C. | C | D. | D |
 能源是现代文明的原动力,通过化学方法可以使能量按人们所期望的形式转化,从而开辟新能源和提高能源的利用率.
能源是现代文明的原动力,通过化学方法可以使能量按人们所期望的形式转化,从而开辟新能源和提高能源的利用率.