题目内容
25 ℃时,0.1 mol Na2CO3与盐酸混合所得的一组体积为1 L的溶液,溶液中部分微粒与pH 的关系如图所示。
下列有关溶液中离子浓度关系叙述正确的是 ( )
| A.W点所示的溶液中:c(Na+)+ c(H+)=2c(CO32-)+ c(OH-)+ c(Cl-) |
| B.pH=4的溶液中:c(H2CO3)+ c(HCO3-)+ c(CO32-)<0.1 mol·L-1 |
| C.pH=8的溶液中:c(H+)+ c(H2CO3)+ c(HCO3-) = c(OH-)+c(Cl-) |
| D.pH=11的溶液中:c(Na+)>c(Cl-)>c(CO32-)>c(HCO3-)>c(H2CO3) |
B
解析试题分析:根据电荷守恒,W点c(Na+)+c(H+)=2c(CO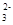 )+c(Cl-)+c(OH-)+c(HCO
)+c(Cl-)+c(OH-)+c(HCO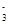 ),A错误;pH=4的溶液中,因为H2CO3部分分解为CO2逸出,“C”的总物质的量小于0.1mol,故B正确;pH=8的溶液中,根据电荷守恒(见A)和溶质Na与C守恒[c(Na+)=2c(CO
),A错误;pH=4的溶液中,因为H2CO3部分分解为CO2逸出,“C”的总物质的量小于0.1mol,故B正确;pH=8的溶液中,根据电荷守恒(见A)和溶质Na与C守恒[c(Na+)=2c(CO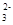 )+2c (H2CO3)+2c(HCO
)+2c (H2CO3)+2c(HCO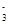 )]得出:c(H+)+c(HCO
)]得出:c(H+)+c(HCO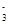 )+2c(H2CO3)=c(Cl-)+c(OH-),C不正确;pH=11的溶液中,根据Na2CO3+HCl===NaHCO3+NaCl和Na2CO3水解可知c(HCO
)+2c(H2CO3)=c(Cl-)+c(OH-),C不正确;pH=11的溶液中,根据Na2CO3+HCl===NaHCO3+NaCl和Na2CO3水解可知c(HCO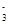 )>c(Cl-),D不正确。
)>c(Cl-),D不正确。
考点:官能团为酯键的芳香化合物的性质。

练习册系列答案
相关题目
下列说法不正确的是
| A.纤维素和乙酸酐作用可生成纤维素三乙酸酯和乙酸 |
B.环戊二烯( )分子中所有碳原子共平面 )分子中所有碳原子共平面 |
C.七叶内酯( )和东莨菪内酯( )和东莨菪内酯( )都是某些中草药中的成分,它们具有相同的官能团,互为同系物 )都是某些中草药中的成分,它们具有相同的官能团,互为同系物 |
D. 该有机物属于单糖,在一定条件下能发生取代、消去、加成、氧化、还原等反应 该有机物属于单糖,在一定条件下能发生取代、消去、加成、氧化、还原等反应 |
分子式为C5H12的烃,其分子内含3个甲基,该烃的二氯代物的同分异构体的数目为
| A.8种 | B.9种 | C.10种 | D.11种 |
丙烯醇在一定条件下可转化为丙烯醛: 。下列有关说法错误的是
。下列有关说法错误的是
| A.丙烯醇与丙醛(CH3CH2CHO)互为同分异构体 |
| B.丙烯醇含有两种官能团 |
| C.可用新制Cu(OH)2鉴别丙烯醛和丙烯醇 |
| D.此转化过程中丙烯醇被还原 |
下列关于有机物的叙述正确的是
| A.甲苯分子中所有原子均在同一个平面上 |
| B.乙烯使KMnO4溶液褪色,是因为两者发生了加成反应 |
| C.分子式为C4H9Br的同分异构体共有4种(不考虑立体异构) |
| D.在酸性条件下,CH3CO18OC2H5的水解产物是CH3CO18OH和C2H5OH |
下列取代基或微粒中,碳原子都满足最外层为8电子结构的是
| A.苯 | B.乙基(—CH2CH3) |
| C.碳正离子[(CH3)3C+] | D.碳烯(CH2) |
分子式为C5H11Cl,在NaOH溶液中加热反应,生成的有机物在Cu的催化作用下加热反应,氧化产物能发生银镜反应的有(不考虑立体异构)( )
| A.2种 | B.4种 | C.6种 | D.8种 |


 的是 ( )
的是 ( )