题目内容
【题目】塑化剂(DEHP)的一种合成路线如下:

已知:①有机物分子中,同一个碳原子上连接两个羟基时不稳定,会自动脱水。
②
请回答下列问题:
(1)DEHP分子的官能团名称___________,B的名称___________。
(2)反应I、IV的类型分别为___________、___________;反应Ⅲ的条件___________。
(3)E的结构简式___________。
(4)反应V的化学方程式___________;
(5)符合下列条件的C的同分异构体共有___________种,写出其中一种的结构简式___________。
①遇FeCl3溶液显紫色 ②能发生银镜反应
③苯环上有三个取代基 ④能与 NaHCO3反应放出CO2气体
(6)请参考上述合成路线,以苯甲醇、正丁醇为原料,无机试剂任选,写出合成G(结构式如右)的路线流程图。合成路线流程图示例如下:
![]()

答:_______________________________________________________。
【答案】酯基 邻苯二甲醛 取代 加成(或还原) Cu、O2、△ 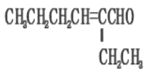 或CH3CH2CH2CH=C(CH2CH3)CHO
或CH3CH2CH2CH=C(CH2CH3)CHO  10
10  (其他合理答案均可)
(其他合理答案均可) 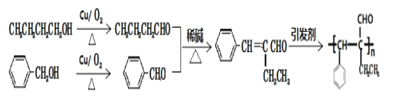
【解析】
![]() 氯气光照发生取代反应生成A(
氯气光照发生取代反应生成A(![]() ),A强碱水溶液条件下水解生成B(
),A强碱水溶液条件下水解生成B(![]() ),B催化氧化生成C(
),B催化氧化生成C(![]() );正丁醇氧化成正丁醛D(
);正丁醇氧化成正丁醛D(![]() ),根据信息可知D在稀碱条件下生成E(
),根据信息可知D在稀碱条件下生成E(![]() ),E与氢气加成生成F(
),E与氢气加成生成F(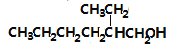 ),C和F酯化反应生成产物DEHP。
),C和F酯化反应生成产物DEHP。
(1)通过观察DEHP分子的结构确定官能团名称;A强碱水溶液条件下水解生成B(![]() )。
)。
(2)反应I是![]() 氯气光照发生取代反应生成A(
氯气光照发生取代反应生成A(![]() );反应IV是 E与氢气加成生成F(
);反应IV是 E与氢气加成生成F(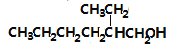 );反应Ⅲ是正丁醇氧化成正丁醛D(
);反应Ⅲ是正丁醇氧化成正丁醛D(![]() ),;
),;
(3) 根据信息可知D在稀碱条件下生成E(![]() );
);
(4)反应V是C和F酯化反应生成产物DEHP;
(5)①遇FeCl3溶液显紫色说明有酚羟基 ②能发生银镜反应说明有醛基
③苯环上有三个取代基 ④能与 NaHCO3反应放出CO2气体,说明有羧基,根据条件寻找同分异构体;
(6)苯甲醇氧化成苯甲醛,正丁醇氧化成正丁醛;苯甲醛和正丁醛根据题干信息生成 ;
; 发生加聚反应生成G(
发生加聚反应生成G(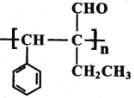 )
)
(1)通过观察DEHP分子的结构确定官能团名称;A强碱水溶液条件下水解生成B(![]() )。
)。
正确答案:酯基 邻苯二甲醛
(2)反应I是![]() 氯气光照发生取代反应生成A(
氯气光照发生取代反应生成A(![]() );反应IV是 E与氢气加成生成F(
);反应IV是 E与氢气加成生成F(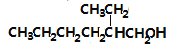 );反应Ⅲ是正丁醇氧化成正丁醛D(
);反应Ⅲ是正丁醇氧化成正丁醛D(![]() );
);
正确答案:取代 加成(或还原) Cu、O2、△
(3) 根据信息可知D在稀碱条件下生成E(![]() );
);
正确答案:
(4)反应V是C和F酯化反应生成产物DEHP,方程式;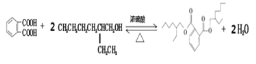 ;
;
正确答案: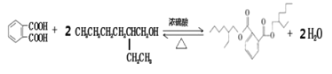
(5)①遇FeCl3溶液显紫色说明有酚羟基 ②能发生银镜反应说明有醛基
③苯环上有三个取代基 ④能与 NaHCO3反应放出CO2气体,说明有羧基,根据条件确定三个官能团羟基、醛基、羧基,采用定二移一法寻找得到10种;
正确答案:10 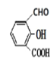 (其他合理答案均可)
(其他合理答案均可)
(6)苯甲醇氧化成苯甲醛,正丁醇氧化成正丁醛;苯甲醛和正丁醛根据题干信息生成 ;
; 发生加聚反应生成G(
发生加聚反应生成G( );
);
正确答案: 。
。

 阅读快车系列答案
阅读快车系列答案







