题目内容
|
下列叙述不正确的是 | |
A. |
在氧化还原反应中,若反应物中有水,则水可能是氧化剂、还原剂、既是氧化剂又是还原剂、既不是氧化剂也不是还原剂 |
B. |
在离子反应中,生成物中离子的总浓度一定比反应物中离子的总浓度小 |
C. |
电解质一定是纯净的化合物 |
D. |
反应物相同的离子反应,离子方程式一定相同 |
答案:BD
解析:
解析:
|
正确解法:在反应物中有水的氧化还原反应中,水可能担当不同的角色.例如:2Na+2H2O 例如:NaHSO4溶液与Ba(OH)2溶液反应,就可能出现下列两种不同的情况.NaHSO4不足时:H++SO42-+Ba2++OH- 点评:在运用分类法时一定要明确分类标准.对于特别绝对的用词,如“一定有”、“一定没有”等要特别的留意,可以采用反例法加以论证. |

练习册系列答案
相关题目
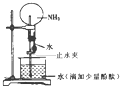 如图是实验室进行氨溶于水的“喷泉实验”的装置,下列叙述不正确的是( )
如图是实验室进行氨溶于水的“喷泉实验”的装置,下列叙述不正确的是( )| A、该实验说明氨气是一种极易溶于水的气体 | B、进入烧瓶中的液体颜色由无色变为红色,说明氨水有碱性 | C、氨水很稳定,将烧瓶中的红色溶液加热,颜色不会发生变化 | D、形成“喷泉”的主要原因是氨气溶于水后,烧瓶内的气压小于大气压 |
苯与乙烯相比较,下列叙述不正确的是( )
| A、都能燃烧,生成二氧化碳和水 | B、都容易发生加成反应 | C、乙烯易发生加成反应,苯只能在特殊条件下才发生加成反应 | D、乙烯易被酸性高锰酸钾溶液氧化,苯不能被酸性高锰酸钾溶液氧化 |