题目内容
氧化还原反应电子得失的表示方法:
(1)用单线桥形式表示下列反应中的电子转移的方向和总数
①Fe+2HCl═FeCl2+H2↑ ②MnO2+4HCl(浓)═MnCl2+Cl2↑+2H2O
(2)用双线桥形式表示下列反应中电子转移的方向和总数
①CuO+H2═Cu+H2O ②2Cl2+2Ca(OH)2═CaCl2+Ca(ClO)2+2H2O.
(1)用单线桥形式表示下列反应中的电子转移的方向和总数
①Fe+2HCl═FeCl2+H2↑ ②MnO2+4HCl(浓)═MnCl2+Cl2↑+2H2O
(2)用双线桥形式表示下列反应中电子转移的方向和总数
①CuO+H2═Cu+H2O ②2Cl2+2Ca(OH)2═CaCl2+Ca(ClO)2+2H2O.
分析:根据化合价升降判断氧化剂和还原剂,结合化学计量数得出得失电子总数,得出正确结论.
解答:解:(1)①Fe:0→+2,↑2,×1
H:-1→0,↓1,×2
 ,
,
②Mn:+4→+2,↓2,×1
Cl:-1→0,↑1,×2
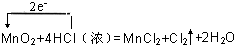 ,
,
故答案为: ,
,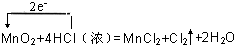 ;
;
(2)①H:0→+1,↑1,×2
Cu:+2→0,↓2,×1
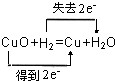 ,
,
②Cl:0→-1,↓1,×2
Cl:0→+1,↑1,×2

故答案为: ,
, .
.
H:-1→0,↓1,×2
 ,
,②Mn:+4→+2,↓2,×1
Cl:-1→0,↑1,×2
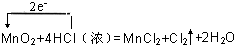 ,
,故答案为:
 ,
,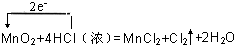 ;
;(2)①H:0→+1,↑1,×2
Cu:+2→0,↓2,×1
 ,
,②Cl:0→-1,↓1,×2
Cl:0→+1,↑1,×2

故答案为:
 ,
, .
.点评:用单线桥或双线桥表示氧化还原反应是基础题型,难度不大,关键是正确判断氧化剂和还原剂.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
下列叙述中正确的是( )
| A、氧化还原反应中得失电子总数一定相等 | B、化学反应前后原子的总数一定不变 | C、电解质溶液中阴阳离子的总数一定相等 | D、分解反应一定是氧化还原反应 |