题目内容
【题目】恒温、恒容的条件下对于N2(g)+3H2(g) ![]() 2NH3(g) ΔH<0的反应,达到化学平衡状态的标志为
2NH3(g) ΔH<0的反应,达到化学平衡状态的标志为
A.断开一个N≡N键的同时有6个N—H键生成
B.混合气体的密度不变
C.混合气体的平均相对分子质量不变
D.N2、H2、NH3分子数之比为1∶3∶2的状态
【答案】C
【解析】
A.断开一个N≡N键的同时有6个N-H键生成,则只表明反应正向进行,不能体现正逆反应速率相等,不能判断平衡状态,故A错误;
B.固定容积的密闭容器中,气体总质量和体积都不变,密度始终不变,不能判断平衡状态,故B错误;
C.该反应反应前后气体物质的量不同,气体质量不变,所以混合气体平均相对分子质量不变能判断平衡状态,故C正确;
D.当体系达平衡状态时,N2、H2、NH3分子数比可能为1:3:2,也可能不是1:3:2,与各物质的初始浓度及转化率有关,不能判断平衡状态,故D错误;
故选:C。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】含碳物质的价值型转化,有利于“减碳”和可持续性发展,有着重要的研究价值。请回答下列问题:
(1)已知CO分子中化学键为C≡O。相关的化学键键能数据如下:
化学键 | H—O | C≡O | C=O | H—H |
E/(kJ·mol1) | 463 | 1075 | 803 | 436 |
CO(g)+H2O(g)CO2(g)+H2(g) ΔH=__kJ·mol1。
下列有利于提高CO平衡转化率的措施有__(填标号)。
a.增大压强 b.降低温度 c.提高原料气中H2O的比例 d.使用高效催化剂
(2)用惰性电极电解KOH溶液,可将空气中的CO2转化为甲酸根(HCOO),然后进一步可以制得重要有机化工原料甲酸。CO2发生反应的电极反应式为__,若电解过程中转移1mol电子,阳极生成气体的体积(标准状况)为__L。
(3)乙苯催化脱氢制取苯乙烯的反应为:
![]() (g)+CO2(g)
(g)+CO2(g)![]() (g)+CO(g)+H2O(g),其反应历程如下:
(g)+CO(g)+H2O(g),其反应历程如下:
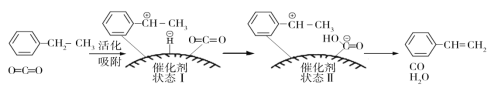
①一定温度下,向恒容密闭容器中充入2mol乙苯和2molCO2,起始压强为p0,平衡时容器内气体总物质的量为5mol,乙苯的转化率为__,用平衡分压代替平衡浓度表示的化学平衡常数Kp=__。[气体分压(p分)=气体总压(p总)×气体体积分数]
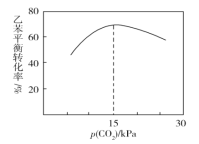
②乙苯平衡转化率与p(CO2)的关系如图所示,请解释乙苯平衡转化率随着p(CO2)变化而变化的原因__。