题目内容
【题目】碳和氮是动植物体中的重要组成元素,向大气中过度排放二氧化碳会造成温室效应,氮氧化物会产生光化学烟雾,目前,这些有毒有害气体的处理成为科学研究的重要内容。
(1)已知热化学方程式:
①2C2H2(g)+5O2(g)===4CO2(g)+2H2O(l) ΔH1
②C(s)+O2(g)===CO2(g) ΔH2
③H2(g)+1/2O2(g)===H2O(l) ΔH3
则反应④2C(s)+H2(g)===C2H2(g)的ΔH=_________。(用含ΔH1、ΔH2、ΔH3的关系式表示)
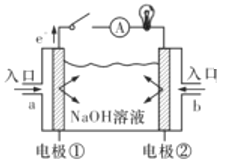
(2)利用上述反应①设计燃料电池(电解质溶液为氢氧化钾溶液),写出电池的负极反应式:___________。
(3)用活性炭还原法可以处理氮氧化物。某研究小组向某密闭容器中加入一定量的活性炭和NO,发生反应C(s)+2NO(g)![]() N2(g)+CO2(g) ΔH<0。在T1℃时,反应进行到不同时间测得各物质的浓度如下:
N2(g)+CO2(g) ΔH<0。在T1℃时,反应进行到不同时间测得各物质的浓度如下:
时间/min 浓度/(mol·L-1) 物质 | 0 | 10 | 20 | 30 | 40 | 50 |
NO | 1.00 | 0.58 | 0.40 | 0.40 | 0.48 | 0.48 |
N2 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
CO2 | 0 | 0.21 | 0.30 | 0.30 | 0.36 | 0.36 |
①1~10 min内,NO的平均反应速率
②30 min后,只改变某一条件,反应重新达到平衡,根据上表中的数据判断改变的条件可能是________(填字母编号)。
a.通入一定量的NO
b.加入一定量的C
c.适当升高反应体系的温度
d.加入合适的催化剂
e.适当缩小容器的体积
【答案】2ΔH2+ΔH3-ΔH1/2 C2H2-10e-+14OH-==2CO32—+8H2O 0.042 mol·L-1·min-1 9/16 < ae
【解析】
(1)根据盖斯定律进行计算;
(2)原电池负极发生氧化反应,电解质溶液为氢氧化钾溶液,C2H2放电生成2CO32-,利用C元素化合价变化判断失去电子数,根据电荷守恒和质量守恒写出电极反应式;
(3)①计算0min~10min内,NO浓度的变化,得到v(NO);20min后达到化学平衡状态,利用化学平衡常数表达式计算,化学平衡常数;
②利用化学平衡状态的特征判断。
(1)已知热化学方程式:①2C2H2(g)+5O2(g)=4CO2(g)+2H2O(l) ΔH1;②C(s)+O2(g)=CO2(g) ΔH2;③H2(g)+1/2O2(g)=H2O(l) ΔH3;则根据盖斯定律可知②×2+③-①×1/2即可得到反应④2C(s)+H2(g)=C2H2(g)的ΔH=2ΔH2+ΔH3-1/2ΔH1,故答案为:2ΔH2+ΔH3-1/2ΔH1。
(2)原电池负极发生氧化反应,电解质溶液为氢氧化钾溶液,C2H2放电生成2CO32-,C元素化合价升高了5,即1molC2H2失去10mole-,电极反应式为:C2H2-10e-+14OH-=2CO32-+8H2O,故答案为:C2H2-10e-+14OH-=2CO32-+8H2O。
(3)①0min~10min内,NO浓度的变化为1.00mol/L-0.58mol/L=0.42mol/L,v(NO)=0.42mol/L÷10min=0.042mol·L-1·min-1,
根据题意和表中数据,20min~30min,40min~50min都是T1℃时的化学平衡,20℃反应达到平衡状态,平衡浓度c(NO)=0.40mol/L,c(N2)=0.3mol/L,c(CO2)=0.30mol/L,C(s)+2NO(g)═N2(g)+CO2(g),平衡常数K1=0.30×0.30/0.402=9/16;
应正反应ΔH<0,温度由T1℃降至T2℃,化学平衡右移,K值增大,所以K1<K2;
故答案为:0.042mol·L-1·min-1;9/16;<。
②30min后,只改变某一条件,反应重新达到平衡,图表数据分析可知一氧化氮,氮气,二氧化碳浓度都增大;
a.通入一定量的NO,反应正向进行,达到平衡后一氧化氮、氮气、二氧化碳浓度增大,故a符合;
b.加入一定量的活性炭是固体,对平衡无影响,故b不符合;
c.升高体系的温度,会使平衡左移,NO浓度增大,而N2、CO2浓度减小,故c不符合;
d.加入合适的催化剂,只能改变化学反应速率,不能改变平衡,浓度不变,故d不符合;
e.适当缩小容器的体积,反应前后是气体体积不变的反应,平衡不动,但个物质浓度增大,符合要求,故e符合。
故答案为:ae。

 云南师大附小一线名师提优作业系列答案
云南师大附小一线名师提优作业系列答案 冲刺100分单元优化练考卷系列答案
冲刺100分单元优化练考卷系列答案