题目内容
科学家制造出一种使用固体电解质的燃料电池,其效率更高,可用于航天航空。如图1所示装置中,以稀土金属材料作惰性电极,在两极上分别通入CH4和空气,其中固体电解质是掺杂了Y2O3的ZrO2固体,它在高温下能传导阳极生成的O2-离子(O2+4e-―→2O2-)。

(1)c电极的名称为 ,d电极上的电极反应式为 。
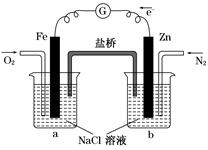
(2)如图2所示用惰性电极电解100 mL 0.5 mol·L-1CuSO4溶液,a电极上的电极反应式为 ,若a电极产生56 mL(标准状况)气体,则所得溶液的pH= (不考虑溶液体积变化),若要使电解质溶液恢复到电解前的状态,可加入 (填序号)。
a.CuO b.Cu(OH)2
c.CuCO3 d.Cu2(OH)2CO3

(1)c电极的名称为 ,d电极上的电极反应式为 。
(2)如图2所示用惰性电极电解100 mL 0.5 mol·L-1CuSO4溶液,a电极上的电极反应式为 ,若a电极产生56 mL(标准状况)气体,则所得溶液的pH= (不考虑溶液体积变化),若要使电解质溶液恢复到电解前的状态,可加入 (填序号)。
a.CuO b.Cu(OH)2
c.CuCO3 d.Cu2(OH)2CO3
(1)正极 CH4+4O2--8e-=CO2↑+2H2O
(2)4OH--4e-=2H2O+O2↑ 1 ac
(2)4OH--4e-=2H2O+O2↑ 1 ac
(1)原电池中电流的方向是从正极流向负极,故c电极为正极;d电极为负极,通入的气体为甲烷,d电极反应式为:CH4+4O2--8e-=CO2+2H2O。
(2)用惰性电极电解CuSO4溶液时,阳极(a电极)反应式:4OH--4e-=2H2O+O2↑;阴极反应式:2Cu2++4e-=2Cu,
n(O2)=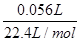 =2.5×10-3mol。
=2.5×10-3mol。
线路中转移电子的物质的量为2.5×10-3 mol×4=0.01 mol,溶液中c(H+)=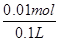 =0.1 mol/L,
=0.1 mol/L,
pH=-lg 0.1=1。加入CuO或CuCO3与溶液中的H+反应,可使电解质溶液恢复到电解前的状态。
(2)用惰性电极电解CuSO4溶液时,阳极(a电极)反应式:4OH--4e-=2H2O+O2↑;阴极反应式:2Cu2++4e-=2Cu,
n(O2)=
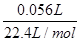 =2.5×10-3mol。
=2.5×10-3mol。线路中转移电子的物质的量为2.5×10-3 mol×4=0.01 mol,溶液中c(H+)=
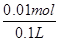 =0.1 mol/L,
=0.1 mol/L,pH=-lg 0.1=1。加入CuO或CuCO3与溶液中的H+反应,可使电解质溶液恢复到电解前的状态。

练习册系列答案
相关题目