题目内容
A—F六种元素中,除C外其他均为短周期元素,它们的原子结构或性质如下表所示:
| 元素 | 结构或性质 |
| A | 原子最外层电子数是内层电子总数的1/5 |
| B | 形成化合物种类最多的元素,其单质为固体 |
| C | 生活中常见的金属,它有两种常见的氯化物,且相对分子质量相差35.5 |
| D | 地壳中含量最多的元素 |
| E | 与D同主族 |
| F | 与E同周期,且最外层电子数等于电子层数 |
(1)A在元素周期表中的位置是 ;A与E形成的化合物的电子式是 。
(2)C的某种氯化物的浓溶液可以腐蚀印刷电路板上的金属铜,此反应的离子方程式是 。
(3)B的单质与D的氢化物在一定条件下反应生成BD和另一产物的化学方程式是 。
(4)F的盐酸盐水溶液呈酸性,原因是 (用离子方程式表示);F的单质与C、D形成的相对分子质量为160的化合物在一定条件下反应的化学方程式是 。
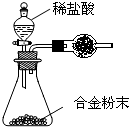
(5)A与F形成的合金是重要的工业材料。某同学仅使用天平和下图所示的装置,粗略测定某些数据即可求出该合金中A元素的含量。(装置中因空气质量引起的误差忽略不计)
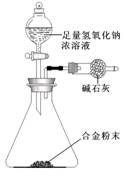
①实验需要测定三个物理量:合金的质量m以及a和b。
a是 ;
b是 。
②合金中A元素的质量分数是 (用含m、a、b的式子表示)。
(1)第3周期,ⅡA族 (1分) 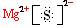 (1分)
(1分)
(2)2Fe3+ + Cu ="=" 2Fe2+ + Cu2+ (2分)
(3)C + H2O 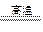 CO + H2 (2分)
CO + H2 (2分)
(4)Al3+ + 3H2O  Al(OH)3 + 3H+ (2分)
Al(OH)3 + 3H+ (2分)
2Al + Fe2O3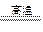 2Fe + Al2O3 (2分)
2Fe + Al2O3 (2分)
(5)①反应前装置和药品的总质量 (1分)
反应后装置和药品的总质量 (1分)
②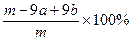 (2分)
(2分)
解析

A—F六种元素中,除C外其他均为短周期元素,它们的原子结构或性质如下表所示:
| 元素 | 结构或性质 |
| A | 原子最外层电子数是内层电子总数的1/5 |
| B | 形成化合物种类最多的元素,其单质为固体 |
| C | 生活中常见的金属,它有两种常见的氯化物,且相对分子质量相差35.5 |
| D | 地壳中含量最多的元素 |
| E | 与D同主族 |
| F | 与E同周期,且最外层电子数等于电子层数 |
请回答下列问题:
(1)A在元素周期表中的位置是 ;A与E形成的化合物的电子式是 。
(2)C的某种氯化物的浓溶液可以腐蚀印刷电路板上的金属铜,此反应的离子方程式是 。
(3)B的单质与D的氢化物在一定条件下反应生成BD和另一产物的化学方程式是 。
(4)F的盐酸盐水溶液呈酸性,原因是 (用离子方程式表示);F的单质与C、D形成的相对分子质量为160的化合物在一定条件下反应的化学方程式是 。
(5)A与F形成的合金是重要的工业材料。某同学仅使用天平和下图所示的装置,粗略测定某些数据即可求出该合金中A元素的含量。(装置中因空气质量引起的误差忽略不计)

①实验需要测定三个物理量:合金的质量m以及a和b。
a是 ;
b是 。
②合金中A元素的质量分数是 (用含m、a、b的式子表示)。
A-F六种元素中,除A外均为短周期元素,它们的原子结构或性质如表所示:
| 序号 | 元素 | 结构或性质 |
| ① | A | 生活中常见的金属,它有两种氯化物,相对分子质量相差35.5 |
| ② | B | 原子最外层电子数是内层电子数的1/5 |
| ③ | C | 形成化合物种类最多的元素之一,其单质为固体 |
| ④ | D | 地壳中含量最多的元素 |
| ⑤ | E | 与D同主族 |
| ⑥ | F | 与E同周期,且最外层电子数等于电子层数 |
(1)E元素在元素周期表中的位置为 。
(2)B与D形成化合物的电子式是 。
(3)CD2能与上述某些元素形成的物质发生置换反应,该反应化学方程式
是 。
(4)A的一种氧化物与F的反应可用于焊接铁轨,写出相关反应的化学方程式:
。
(5)F元素的氧化物溶于浓NaOH溶液的离子方程式:
。
A-F六种元素中,除A外均为短周期元素,它们的原子结构或性质如表所示:
|
序号 |
元素 |
结构或性质 |
|
① |
A |
生活中常见的金属,它有两种氯化物,相对分子质量相差35.5 |
|
② |
B |
原子最外层电子数是内层电子数的1/5 |
|
③ |
C |
形成化合物种类最多的元素之一,其单质为固体 |
|
④ |
D |
地壳中含量最多的元素 |
|
⑤ |
E |
与D同主族 |
|
⑥ |
F |
与E同周期,且最外层电子数等于电子层数 |
(1)E元素在元素周期表中的位置为 。
(2)B与D形成化合物的电子式是 。
(3)CD2能与上述某些元素形成的物质发生置换反应,该反应化学方程式
是 。
(4)A的一种氧化物与F的反应可用于焊接铁轨,写出相关反应的化学方程式:
。
(5)F元素的氧化物溶于浓NaOH溶液的离子方程式:
。
 A-F六种元素中,除A外均为短周期元素,它们的原子结构或性质如表所示:
A-F六种元素中,除A外均为短周期元素,它们的原子结构或性质如表所示: