题目内容
【题目】光伏材料是指能将太阳能直接转换成电能的材料。光伏材料又称太阳能材料,只有半导体材料具有这种功能。可做太阳电池材料的有单晶硅、多晶硅、非晶硅、GaAs、GaAlAs、InP、CdS、CdTe、CuInSe等。
(1)Se在周期表的位置为_____,硅的基态原子电子排布式为_____,基态Ga原子核外电子占据的最高能级为_____,铜的基态原子价电子排布图为______。
(2)P、S、Ga电负性从大到小的顺序为____________________。
(3)与Al元素在元素周期表中处于对角线的铍,在性质上具有相似性,请写出铍的氧化物与氢氧化钠溶液反应的离子方程式_______________________
(4)As元素的第一电离能_____Se元素的第一电离能(填“大于”、“小于”或“等于”),原因是_______________。
(5)太阳电池材料的很多金属或金属化合物在灼烧时会产生特殊的火焰颜色,请用原子结构的知识阐述产生此现象的原因是_________________________
【答案】第四周期VIA族 1s22s22p63s23p2 4p  S>P>Ga BeO+2OH﹣═BeO22﹣+H2O 大于 As元素4p能级为半满稳定状态,能量较低,第一电离能高于同周期相邻的Se元素 电子跃迁时会伴随着能量变化,该能量主要以特定波长的光的形式体现,因而很多金属或金属化合物在灼烧时会呈现特殊的火焰颜色
S>P>Ga BeO+2OH﹣═BeO22﹣+H2O 大于 As元素4p能级为半满稳定状态,能量较低,第一电离能高于同周期相邻的Se元素 电子跃迁时会伴随着能量变化,该能量主要以特定波长的光的形式体现,因而很多金属或金属化合物在灼烧时会呈现特殊的火焰颜色
【解析】
(1)Se为34号元素在周期表的位置为第四周期VIA族,硅为14元素,基态原子电子排布式为1s22s22p63s23p2, Ga为31号元素,核外电子排布式为:1s22s22p63s23p63d104s24p1,基态原子核外电子占据的最高能级为4p,铜为29号元素,核外电子排布式为1s22s22p63s23p63d104s1,基态原子价电子排布图为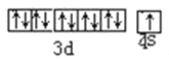 。
。
答案为:第四周期VIA族 (2). 1s22s22p63s23p2 (3). 4p (4).  ;
;
(2)非金属性越强,电负性越强,非金属性:S>P>Ga,则电负性从大到小的顺序为S>P>Ga。
答案为:S>P>Ga;
(3)Al2O3与NaOH溶液反应的离子方程式为:Al2O3+2OH=2AlO2+H2O,因Be与Al的性质具有相似性,类比可知,Be的最高价氧化物对应的水化物与NaOH溶液反应的离子方程式为:BeO+2OH﹣═BeO22﹣+H2O,
故答案为:BeO+2OH﹣═BeO22﹣+H2O;
(4)As为33号元素,核外电子排布式为1s22s22p63s23p63d104s24p3,Se的核外电子排布式:1s22s22p63s23p63d104s24p4,As的4p轨道处于半充满状态更稳定,故As元素的第一电离能大于Se元素的第一电离能;
答案为:大于;As元素4p能级为半满稳定状态,能量较低,第一电离能高于同周期相邻的Se元素
(5)电子跃迁时会伴随着能量变化,该能量主要以特定波长的光的形式体现,因而很多金属或金属化合物在灼烧时会呈现特殊的火焰颜色;
答案为:电子跃迁时会伴随着能量变化,该能量主要以特定波长的光的形式体现,因而很多金属或金属化合物在灼烧时会呈现特殊的火焰颜色。

 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案