题目内容
【题目】某研究性学习小组根据反应2KMnO4+10FeSO4+8H2SO4===2MnSO4+5Fe2(SO4)3+K2SO4+8H2O设计如下原电池,其中甲、乙两烧杯中各物质的物质的量浓度均为1 mol·L-1,溶液的体积均为200 mL,盐桥中装有饱和K2SO4溶液。
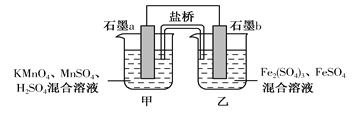
回答下列问题:
(1)此原电池的负极是石墨__________(填“a”或“b”),发生__________反应。
(2)请写出甲烧杯中的电极反应式___________________________________________。(3)若不考虑溶液的体积变化,MnSO4浓度变为1.6 mol·L-1,则反应中转移的电子为__________mol。
【答案】 b 氧化 MnO+5e-+8H+===Mn2++4H2O 0.6
【解析】本题主要考查原电池原理。
(1)乙烧杯中Fe2+失去电子被氧化,所以此原电池的负极是石墨b,发生氧化反应。
(2)甲烧杯中的电极反应式为MnO+5e-+8H+===Mn2++4H2O。
(3)若不考虑溶液的体积变化,MnSO4增加0.2L×(1.6-1)mol·L-1=0.12mol,MnSO4~5e-,则反应中转移的电子为0.6mol。

练习册系列答案
相关题目