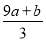题目内容
X、Y、Z、Q、W、R六种短周期元素原子序数依次增大。化合物甲由X、Z、Q三种元素组成,常温下0.1 mol/L甲溶液的pH=13。工业上常用电解饱和QR溶液生成甲;化合物乙由X、R两种元素组成。请回答下列问题:
(1)Q的原子结构示意图为________。
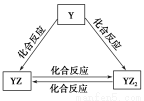
(2)Y元素的单质能发生如图所示的转化,则Y元素为________(填元素符号)。
在甲溶液中通入足量YZ2气体,所得溶液呈碱性,原因是__________________(用离子方程式和必要的文字说明)。
(3)W的单质既能与甲溶液反应,又能与乙溶液反应。
①常温下,将W的单质和甲溶液混合,发生反应的离子方程式为______________________________________________________________________________;
②Q、W两种元素金属性的强弱为Q________W(填“<”或“>”),下列表述中能证明这一事实的是________(填序号)。
a.Q单质的熔点比W单质的低
b.Q的最高价氧化物的水化物的碱性比W的最高价氧化物的水化物的碱性强
c.W的原子序数大
(1)
(2)C 足量CO2通入NaOH溶液中生成NaHCO3,HCO3- H++CO32-,HCO3-+H2O
H++CO32-,HCO3-+H2O H2CO3+OH-,HCO3-的水解程度大于其电离程度,故呈碱性
H2CO3+OH-,HCO3-的水解程度大于其电离程度,故呈碱性
(3)①2Al+2OH-+2H2O=2AlO2-+3H2↑ ②> b
【解析】(1)化合物甲由X、Z、Q三种元素组成,常温下0.1 mol/L甲溶液的pH=13,说明甲溶液呈碱性,且为强碱,因为其完全电离,又因为X、Z、Q均为短周期元素,且原子序数依次增大,故确定为NaOH。则X为H、Z为O、Q为Na。(2)因为Y在元素周期表中介于H和O之间,又根据框图分析,Y可以与氧气反应分别生成YO和YO2,故Y可能为碳元素或氮元素,但框图中指明YO2可以发生化合反应生成YO,所以确定Y为碳元素。向氢氧化钠溶液中通入足量二氧化碳可得到碳酸氢钠溶液,碳酸氢根离子的水解能力大于其电离能力,故溶液呈碱性。(3)由W的单质既能与甲溶液反应,又能与乙溶液反应,且乙由X、R两种元素组成,可知乙溶液为酸,从而推出W是Al。

化学学科中的化学平衡、电离平衡、水解平衡和溶解平衡均符合勒夏特列原理。
请回答下列问题:
 (1)工业上采取CO和H2为原料合成乙醇,其化学反应方程式为:2CO(g)+4H2(g)??
(1)工业上采取CO和H2为原料合成乙醇,其化学反应方程式为:2CO(g)+4H2(g)??
CH3CH2OH(g)+H2O(g)。请写出该反应的化学平衡常数表达式K=________。
(2)常温下,浓度均为0.1 mol·L-1的六种溶液的pH如下表:
溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN | Na2SO4 |
pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 | 7.0 |
①上述盐溶液中的阴离子,结合质子能力最强的是________。
②根据表中数据,浓度均为0.01 mol·L-1的下列五种物质的溶液中,酸性最强的是________(填字母);将各溶液分别稀释100倍,pH变化最小的是________(填字母)。
A.HCN B.HClO C.H2SO4 D.CH3COOH E.H2CO3
③把CO2气体通入饱和碳酸钠溶液中,可以观察到的现象为________,原因为________(用离子方程式表示)。
④要增大氯水中HClO的浓度,可向氯水中加入少量的碳酸钠溶液,反应的离子方程式为____________。
(3)某温度时,BaSO4在水中的沉淀溶解平衡曲线如图所示。下列说法错误的是_______。

A.加入适量BaCl2(固体)可以使溶液由d点变到c点
B.通过加水稀释可以使溶液由b点变到a点
C.d点无BaSO4沉淀生成
D.a点对应的Ksp等于c点对应的Ksp