题目内容
【题目】若往20mL 0.01molL﹣l HNO2(弱酸)溶液中逐滴加入一定浓度的烧碱溶液,测得混合溶液的温度变化如图所示,下列有关说法不正确的是( ) 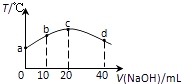
A.HNO2的电离平衡常数:c点>b点
B.b点混合溶液显酸性:c(Na+)>c(NO2﹣)>c(H+)>c(OH﹣)
C.c点混合溶液中:c(OH﹣)>c(HNO2)
D.d点混合溶液中:c(Na+)>c(OH﹣)>c(NO2﹣)>c(H+)
【答案】B
【解析】解:A、HNO2的电离是吸热过程,温度越高电离平衡常数越大,而c高于b,所以电离平衡常数:c点>b点,故A正确; B、b点得到HNO2 , 和NaNO2混合溶液显酸性,说明电离大于水解,所以离子浓度大小为:c(NO2﹣)>c(Na+)>c(H+)>c(OH﹣),故B错误;
C、a→c温度升高说明两者恰好完全中和,点两者恰好完全反应,而c→d温度降低,所水解为主,所以c点得到NaNO2溶液是强碱弱酸盐,水解溶液呈碱性,所以c(OH﹣)>c(HNO2),故C正确;
D、d点混合溶液中当c(NaOH)较大时,得到NaOH和NaNO2混合溶液,所以离子的浓度为:c(Na+)>c(OH﹣)>c(NO2﹣)>c(H+),故D正确;
故选B.
A、HNO2的电离是吸热过程,温度越高电离平衡常数越大;
B、b点得到HNO2 , 和NaNO2混合溶液显酸性,说明电离大于水解,由此分析解答,也可能结合电荷守恒分析;
C、a→c温度升高说明两者恰好完全中和,点两者恰好完全反应,而c→d温度降低,所水解为主;
D、d点混合溶液中当c(NaOH)较大时,得到NaOH和NaNO2混合溶液.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目