题目内容
下列关于浓硝酸和浓硫酸的性质叙述不正确的是( )
| A、都能在加热情况下与C反应生成CO2 |
| B、都能做干燥剂 |
| C、常温下都能用铁质容器盛装 |
| D、在与金属反应时都既表现出氧化性,有表现出酸性 |
考点:硝酸的化学性质,浓硫酸的性质
专题:元素及其化合物
分析:A.浓硫酸和浓硝酸都具有强氧化性,在加热条件下都能氧化碳单质生成二氧化碳;
B.浓硝酸没有吸水性,不能作干燥剂;
C.常温下,浓硫酸和浓硝酸与铁发生钝化现象;
D.与金属反应时生成硝酸盐或硫酸盐,同时有氮氧化物或二氧化硫生成,根据化合价变化确定酸的性质.
B.浓硝酸没有吸水性,不能作干燥剂;
C.常温下,浓硫酸和浓硝酸与铁发生钝化现象;
D.与金属反应时生成硝酸盐或硫酸盐,同时有氮氧化物或二氧化硫生成,根据化合价变化确定酸的性质.
解答:
解:A.C+2H2SO4(浓)
2SO2↑+CO2↑+2H2O、C+4HNO3(浓)
CO2↑+4NO2↑+2H2O,所以在加热条件下都能氧化碳单质生成二氧化碳,故A正确;
B.浓硝酸有挥发性但没有吸水性,所以浓硝酸不能作干燥剂,浓硫酸具有吸水性,能作干燥剂,故B错误;
C.常温下,铁和浓硫酸或浓硝酸反应生成一层致密的氧化物薄膜而阻止进一步被氧化,该现象为钝化现象,所以常温下都能用铁质容器盛装,故C正确;
D.与金属反应时生成硝酸盐或硫酸盐,同时有氮氧化物或二氧化硫生成,该反应中部分酸根离子化合价不变、部分酸根离子化合价升高,所以酸体现氧化性和酸性,故D正确;
故选B.
| ||
| ||
B.浓硝酸有挥发性但没有吸水性,所以浓硝酸不能作干燥剂,浓硫酸具有吸水性,能作干燥剂,故B错误;
C.常温下,铁和浓硫酸或浓硝酸反应生成一层致密的氧化物薄膜而阻止进一步被氧化,该现象为钝化现象,所以常温下都能用铁质容器盛装,故C正确;
D.与金属反应时生成硝酸盐或硫酸盐,同时有氮氧化物或二氧化硫生成,该反应中部分酸根离子化合价不变、部分酸根离子化合价升高,所以酸体现氧化性和酸性,故D正确;
故选B.
点评:本题考查了浓硫酸和浓硝酸的性质,知道二者的相似性和区别是解本题关键,二者都是强氧化性酸,知道钝化原理,为易错点.

练习册系列答案
相关题目
下列有关叙述正确的是( )
| A、测定中和热时,大小两烧杯间填满碎纸的作用是固定小烧杯 |
| B、若用0.010mo1?L-1的氢氧化钠标准溶液滴定未知浓度的盐酸时,滴定前滴定管尖嘴处有气泡,滴定后气泡消失,则测定结果偏小 |
| C、在中和滴定实验中,滴定管用蒸馏水洗涤后,再用标准液润洗,再加进标准液 |
| D、进行中和滴定操作时,左手震荡锥形瓶,右手转动活塞控制液滴流速,眼睛要始终注视滴定管内溶液液面的变化 |
下列反应的离子方程式书写正确的是( )
A、用银氨溶液检验乙醛中的醛基:CH3CHO+2Ag(NH3)2++2OH-
| ||
| B、用二氧化硫水溶液吸收溴蒸气:SO2+Br2+2H2O=2H++SO42-+2HBr | ||
| C、在(NH4)2SO4溶液中逐滴加入少量的Ba(OH)2溶液:NH4++SO42-+Ba2++OH-=BaSO4↓+NH3?H2O | ||
| D、次氯酸钙溶液中通入少量SO2气体:Ba2++2ClO-+SO2+H2O=CaSO3↓+2HClO |
阿魏酸在食品、医药等方面有着广泛用途.一种合成阿魏酸的反应可表示为
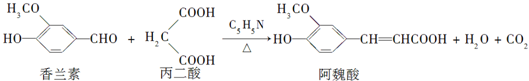
下列说法正确的是( )

下列说法正确的是( )
| A、可用酸性KMnO4溶液检测上述反应是否有阿魏酸生成 |
| B、与香兰素互为同分异构体,分子中有4种不同化学环境的氢,且能发生银镜反应的酚类化合物共有3种 |
| C、通常条件下,香兰素、阿魏酸都能发生取代、加成、消去反应 |
| D、香兰素、阿魏酸均可与Na2CO3、NaOH溶液反应 |
已知反应:2M(g)+N(g)+P(g)
2Q(g)+3R(g)△H>0,在恒容的密闭容器中,下列有关说法正确的是( )
| 180℃ |
| 催化剂 |
| A、平衡时,其他条件不变,增加M的浓度,N的转化率减小 |
| B、平衡时,其他条件不变,升高温度可使该反应的平衡常数增大 |
| C、单位时间内消耗N和Q的物质的量比为1:1时,反应达到平衡 |
| D、其他条件不变,使用高效催化剂,N和P的转化率增大 |