题目内容
下列各组物质中,因为反应条件或用量不同而发生不同化学反应的是
①澄清石灰水和CO2 ②Na与O2
③AlCl3溶液与氨水 ④Fe与稀HNO3
| A.除②外 | B.除③外 | C.除②③外 | D.除③④外 |
B
解析试题分析:①少量二氧化碳和澄清石灰水反应生成碳酸钙,过量二氧化碳和澄清石灰水反应生成生成碳酸氢钙,正确;②Na与O2反应在不同条件下产物不同;钠在氧气中加热条件下反应生成过氧化钠,常温下反应生成氧化钠,产物不同,正确;③氯化铝溶液和氨水反应生成氢氧化铝沉淀;氢氧化铝和弱碱不反应,错误;④Fe与稀HNO3,铁少量生成硝酸铁,铁过量生成硝酸亚铁,正确;综上所述,选B。
考点:考查元素化合物知识。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
下列陈述I、II正确并且有因果关系的是
| 选项 | 陈述I | 陈述II |
| A | 浓H2SO4有吸水性 | 浓H2SO4可用于干燥氨气 |
| B | SO2有还原性 | SO2尾气可用NaOH溶液吸收 |
| C | Mg有还原性 | 电解MgCl2饱和溶液可制备Mg |
| D | 锌金属活动性比铁强 | 海轮外壳上装锌块可减缓腐蚀 |
下列关于元素及其化合物的说法正确的是
| A.Fe在常温下可与浓硝酸、稀硝酸、浓硫酸剧烈反应 |
| B.Al、Cl2均能和NaOH溶液发生氧化还原反应,且两单质的作用相同 |
| C.Na久置于空气中,可以和空气中的有关物质发生反应,最终生成Na2CO3 |
| D.制备FeCl3、CuCl2固体均可采用将溶液直接蒸干的方法 |
下列有关物质性质的应用正确的是
| A.浓硫酸有吸水性,可用于干燥氨气和二氧化硫 |
| B.明矾溶于水能形成胶体,可用于自来水的杀菌消毒 |
| C.常温下铁能被浓硝酸钝化,可用铁质容器贮运浓硝酸 |
| D.金属钠具有强还原性,可用与TiCl4溶液反应制取金属Ti |
下列各组物质所发生的化学反应中,由于反应物的用量不同而得到不同产物的是
①铁与稀硝酸 ②硫酸铜溶液与氨水 ③碳酸钠溶液与稀盐酸 ④铁与氯气
| A.①②③ | B.①②③④ | C.②③ | D.③④ |
不论以何种比例混合,将甲和乙两种混合气体同时通入过量的丙溶液中,一定能产生沉淀的组合是( )
| 序号 | 甲 | 乙 | 丙 |
| ① | CO2 | SO2 | 石灰水 |
| ② | HCl | CO2 | 石灰水 |
| ③ | CO2 | SO2 | Ba(NO3)2 |
| ④ | NO2 | SO2 | BaCl2 |
| ⑤ | CO2 | NH3 | CaCl2 |
A.①③④ B.②③④⑤ C.①②③④ D.①②④
下列转化关系在给定条件下不能实现的是 ( )。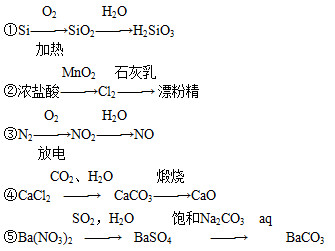
| A.①②③ | B.②③⑤ | C.③④⑤ | D.①②③④ |
下列物质的转化在给定条件下能实现的是( )
①Al2O3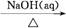 NaAlO2(aq)
NaAlO2(aq)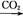 Al(OH)3
Al(OH)3
②S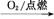 SO3
SO3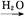 H2SO4
H2SO4
③Fe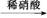 Fe2+
Fe2+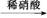 Fe3+
Fe3+
④Fe2O3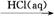 FeCl3(aq)
FeCl3(aq)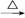 无水FeCl3
无水FeCl3
⑤MgCl2(aq)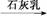 Mg(OH)2
Mg(OH)2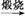 MgO
MgO
| A.①③⑤ | B.②③④ | C.②④⑤ | D.①④⑤ |
下列实验不能达到目的的是 ( )。
| A.用AlCl3溶液和过量氨水制备Al(OH)3 |
| B.用NH4Cl和Ca(OH)2固体混合加热制备NH3 |
| C.用NaOH溶液除去苯中的溴 |
| D.用足量铜粉除去FeCl2溶液中的FeCl3杂质 |