题目内容
NA表示阿伏加德罗常数的值,下列说法正确的是
- A.0.1mol/L的100mL FeCl3溶液中,含有的离子数为0.04NA
- B.标准状况下,将m1克锌加入到m2克20%的盐酸中放出nLH2,则转移电子数为nNA/11.2
- C.9gD2O中含有的电子数为5NA
- D.120g由NaHSO4和KHSO3组成的混合物中共含有3NA的阴阳离子
B
分析:A、铁离子水解生成氢氧化铁和氢离子,溶液中离子数增多;
B、锌和氯化氢的量不能确定,依据化学反应生成氢气计算电子转移;
C、依据n= ,结合分子式计算电子数;
,结合分子式计算电子数;
D、NaHSO4和KHSO3的摩尔质量相同,120g混合物依据n= ,计算得到物质的量,硫酸氢钠是钠离子和硫酸氢根离子构成,亚硫酸氢钾是钾离子和亚硫酸氢根离子构成;
,计算得到物质的量,硫酸氢钠是钠离子和硫酸氢根离子构成,亚硫酸氢钾是钾离子和亚硫酸氢根离子构成;
解答:A、0.1mol/L的100mL FeCl3溶液中,Fe3++3H2O?Fe(OH)3+3H+,含有的离子数大于0.04NA,故A错误;
B、标准状况下,将m1克锌加入到m2克20%的盐酸中放出nLH2,锌和氯化氢的量不能确定,依据化学反应生成氢气计算,2H+~H2~2e-,转移电子数 ×2×NA=
×2×NA= ,故B正确;
,故B正确;
C、9gD2O物质的量= =
=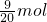 ,分子中含有的电子数=
,分子中含有的电子数=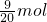 ×10×NA=4.5NA ,故C错误;
×10×NA=4.5NA ,故C错误;
D、NaHSO4和KHSO3的摩尔质量相同为120g/mol,120g由NaHSO4和KHSO3物质的量为1mol,硫酸氢钠是钠离子和硫酸氢根离子构成,亚硫酸氢钾是钾离子和亚硫酸氢根离子构成;,组成的混合物中共含有2NA的阴阳离子,故D错误;
故选B.
点评:本题考查了阿伏伽德罗常数的应用,主要考查盐类水解生成两种数的特征,气体摩尔体积的条件应用,氧化还原反应电子转移,混合物的组成特征分析,题目难度中等.
分析:A、铁离子水解生成氢氧化铁和氢离子,溶液中离子数增多;
B、锌和氯化氢的量不能确定,依据化学反应生成氢气计算电子转移;
C、依据n=
 ,结合分子式计算电子数;
,结合分子式计算电子数;D、NaHSO4和KHSO3的摩尔质量相同,120g混合物依据n=
 ,计算得到物质的量,硫酸氢钠是钠离子和硫酸氢根离子构成,亚硫酸氢钾是钾离子和亚硫酸氢根离子构成;
,计算得到物质的量,硫酸氢钠是钠离子和硫酸氢根离子构成,亚硫酸氢钾是钾离子和亚硫酸氢根离子构成;解答:A、0.1mol/L的100mL FeCl3溶液中,Fe3++3H2O?Fe(OH)3+3H+,含有的离子数大于0.04NA,故A错误;
B、标准状况下,将m1克锌加入到m2克20%的盐酸中放出nLH2,锌和氯化氢的量不能确定,依据化学反应生成氢气计算,2H+~H2~2e-,转移电子数
 ×2×NA=
×2×NA= ,故B正确;
,故B正确;C、9gD2O物质的量=
 =
=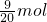 ,分子中含有的电子数=
,分子中含有的电子数=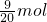 ×10×NA=4.5NA ,故C错误;
×10×NA=4.5NA ,故C错误;D、NaHSO4和KHSO3的摩尔质量相同为120g/mol,120g由NaHSO4和KHSO3物质的量为1mol,硫酸氢钠是钠离子和硫酸氢根离子构成,亚硫酸氢钾是钾离子和亚硫酸氢根离子构成;,组成的混合物中共含有2NA的阴阳离子,故D错误;
故选B.
点评:本题考查了阿伏伽德罗常数的应用,主要考查盐类水解生成两种数的特征,气体摩尔体积的条件应用,氧化还原反应电子转移,混合物的组成特征分析,题目难度中等.

练习册系列答案
 期末宝典单元检测分类复习卷系列答案
期末宝典单元检测分类复习卷系列答案
相关题目