题目内容
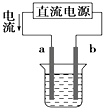
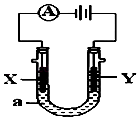
【题目】如图所示,E池中加入0.1mol/L CuCl2 溶液,F池中加入0.1mol/L AgNO3 溶液,将四个铂电极串联起来通电,则a,b,c,d 四电极上所产生的物质,其物质的量之比为( ) 
A.2:2:4:1
B.1:1:2:1
C.2:1:l:1
D.2:2:2:1
【答案】A
【解析】解:根据电解方程式:E池中,阳极电极反应式为:2Cl﹣﹣2e﹣=Cl2↑,阴极电极反应式为:Cu2++2e﹣=Cu;F池中,阳极发生4OH﹣﹣4e﹣=2H2O+O2↑,阴极Ag++e﹣=Ag,据电子守恒,假设转移4mol电子,E池中阳极b生成2mol氯气,阴极a生成2molCu,F池中阳极d生成1mol氧气,阴极c生成4molAg,所以a、b、c、d四个电极上所析出的物质的物质的量之比是2:2:4:1,故选A.

练习册系列答案
相关题目
【题目】A、B、C、D四种可溶性物质,都是由下表中的离子形成的.
阳离子 | Ba2+ | Ag+ | Na+ | Cu2+ |
阴离子 | NO3﹣ | SO42﹣ | OH﹣ | CO32﹣ |
已知每种物质中阴阳离子互不重复.
①若把四种物质分别溶解于盛有蒸馏水的四支试管中,只有C溶液呈蓝色.
②若向①的四支试管中分别加盐酸,B溶液有沉淀产生,D溶液有无色无味的气体逸出.
(1)根据①②实验事实可推断它们的化学式为:A , B , C , D .
(2)写出下列反应的离子方程式:a.A溶液与C溶液混合:
b.向A溶液中加入NaHSO4溶液至Ba2+恰好沉淀完全: .