题目内容
SF6是一种优良的绝缘气体,分子结构中只存在S-F键。已知:1molS(s)转化为气态硫原子吸收能量280 kJ,断裂1molF-F 、S-F键需吸收的能量分别为160 kJ、330 kJ。则S(s)+3F2(g)=SF6(g)的反应热△H为
| A.-1780kJ/mol | B.-1220 kJ/mo | C.-450 kJ/mol | D.+430 kJ/mol |
B
解析试题分析:对于S(s)+3F2(g)═SF6(g),SF6是一种优良的绝缘气体,分子结构中只存在S-F键,由△H=反应物总键能-生成物总键能,所以其反应热△H=280KJ/mol+3×160KJ/mol-6×330KJ/mol=-1220kJ/mol,故选B。
考点:考查反应热的计算

 全优考典单元检测卷及归类总复习系列答案
全优考典单元检测卷及归类总复习系列答案化学反应一般均会伴随着能量变化,对H2在O2中燃烧的反应,正确的是
| A.该反应为吸热反应 | B.该反应为放热反应 |
| C.断裂H-H键放出能量 | D.生成H-O键吸收能量 |
金刚石和石墨都是碳的单质,石墨在一定条件下可以转化为金刚石并需要吸收能量,已知12克石墨或金刚石完全燃烧时放出的热量依次为Q1和Q2,下列说法错误的是( )
| A.Q1<Q2 |
| B.石墨不如金刚石稳定 |
| C.质量相等的石墨与金刚石,石墨具有的能量比金刚石低 |
| D.质量相等的石墨与金刚石完全燃烧,生成的二氧化碳一样多 |
已知25℃、101kPa条件下:
4Al (s) + 3O2 (g)=2Al2O3 (s) △H=-2834.9 kJ/mol
4Al (s) + 2O3 (g) = 2Al2O3 (s) △H= -3119.91kJ/mol
由此得出的结论正确的是
| A.等质量的O2比O3能量低,由O2变O3为放热反应 |
| B.等质量的O2比O3能量低,由O2变O3 为吸热反应 |
| C.3O2(g)=2O3 (g)△H=285.0 kJ/mol |
| D.O3比O2稳定,由O2变O3 为吸热反应 |
某反应的反应过程中能量变化如图所示(图中E1表示正反应的活化能,E2表示逆反应的活化能)。下列有关叙述正确的是( ) 
| A.该反应为放热反应 |
| B.该反应焓变可表示为△H=-(E1-E2)kJ·mol-1 |
| C.催化剂能降低反应的活化能 |
| D.催化剂能改变反应的焓变 |
用Cl2生产某些含氯有机物时会产生副产物HCl。 利用反应A:4HCl+O2 2Cl2+2H2O,
2Cl2+2H2O,
可实现氯的循环利用。
已知:Ⅰ.反应A中,4mol HCl被氧化,放出115.6kJ的热量.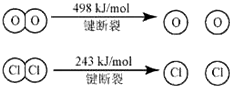
Ⅱ.则断开1 mol H—O键与断开1 mol H—Cl键所需能量相差约为
| A.16kJ | B.24kJ | C.32kJ | D.48kJ |
下列有关中和热的说法正确的是( )
| A.表示中和热的热化学方程式:H+(l)+OH-(l)=H2O(l) ΔH=-57.3 kJ/mol |
| B.准确测量中和热的实验过程中,至少需测定温度4次 |
| C.中和热的实验过程中,环形玻璃搅拌棒材料若用铜代替,则测量出的中和热数值偏小 |
| D.已知2NaOH(aq)+H2SO4(aq)=Na2SO4(aq)+2H2O(l) ΔH=-114.6 kJ/mol,则该反应的中和热为114.6 kJ/mol |
化学与环境、能源、材料和科技等密切相关。下列说法中不正确的是( )
| A.鼓励汽车、家电“以旧换新”,可提高能源利用效率,与环境保护基本无关系 |
| B.农村大力发展沼气,将废弃的秸秆转化为清洁高效的能源 |
| C.镁铝合金可用作制造飞机的材料 |
| D.氢氧燃料电池要广泛地应用于实际生产、生活中,高容量储氢材料的研制是需解决 |
常温下,已知:
4Al(s)+3O2(g)=2Al2O3(s)ΔH1
4Fe(s)+3O2(g)=2Fe2O3(s)ΔH2
下面关于ΔH1、ΔH2的比较正确的是( )
| A.ΔH1>ΔH2 | B.ΔH1<ΔH2 |
| C.ΔH1=ΔH2 | D.无法计算 |