题目内容
将20mL充满NO和NO2混合气体的试管倒立于水中,过一会儿,当试管内有6mL水上升时,液面不再变化.原混合气体中NO和NO2的体积比为(在相同条件下)( )
| A、9:11 | B、7:3 | C、11:9 | D、3:7 |
分析:将20mL充满NO和NO2混合气体的试管倒立于水中,过一会儿,当试管内有6mL水上升时,液面不再变化,说明气体体积减少6ml,体积减少是反应3NO2+H2O=2HNO3+NO前后气体体积变化造成的,每3体积NO2通入水中会生成1体积NO,减少2体积气体体积,题给反应气体体积变化为6ml,说明参加反应的NO2气体体积为9ml,则原气体中NO气体体积为11ml,所以原混合气体中NO和NO2的体积比为11:9.
解答:解:将20mL充满NO和NO2混合气体的试管倒立于水中,过一会儿,当试管内有6mL水上升时,液面不再变化,说明气体体积减少6ml,根据化学反应计算如下:
3NO2+H2O=2HNO3+NO△V(气体体积减少)
3 2
V(NO2) 6ml
求得:V(NO2)=9ml,
原气体中V(NO)=20-9=11ml,
所以原混合气体中NO和NO2的体积比为为V(NO):V(NO2)=11ml:9ml=11:9;
故选C.
3NO2+H2O=2HNO3+NO△V(气体体积减少)
3 2
V(NO2) 6ml
求得:V(NO2)=9ml,
原气体中V(NO)=20-9=11ml,
所以原混合气体中NO和NO2的体积比为为V(NO):V(NO2)=11ml:9ml=11:9;
故选C.
点评:本题考查了氮氧化物溶于水的有关计算,重点考查了氮氧化物的化学性质和差量计算的运用,题目难度中等.

练习册系列答案
 小学夺冠AB卷系列答案
小学夺冠AB卷系列答案 ABC考王全优卷系列答案
ABC考王全优卷系列答案
相关题目
将5mL NO和15mL 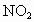 的混合气体,通入倒置水槽充满水的试管中,最后在试管中能收集的气体体积是
的混合气体,通入倒置水槽充满水的试管中,最后在试管中能收集的气体体积是
[ ]
|
A.20mL |
B.15mL |
|
C.10mL |
D.5mL |
将5mL NO和15mL 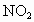 的混合气体,通入倒置水槽充满水的试管中,最后在试管中能收集的气体体积是
的混合气体,通入倒置水槽充满水的试管中,最后在试管中能收集的气体体积是
[ ]
|
A.20mL |
B.15mL |
|
C.10mL |
D.5mL |