题目内容
【题目】铝、铁是常见的两种金属,它们的单质及化合物在生活生产中处处可见。
(1)过量的铁和稀硝酸发生反应,产物是![]() 和
和![]() ,写出该反应的化学方程式_______________。
,写出该反应的化学方程式_______________。
(2)实验室配制![]() 溶液时,如果没有隔绝空气,
溶液时,如果没有隔绝空气,![]() 会被氧化为________(填写化学式)。在该溶液中加入________试剂,看到_________现象,证明溶液变质。写出检验
会被氧化为________(填写化学式)。在该溶液中加入________试剂,看到_________现象,证明溶液变质。写出检验![]() 已经被氧化的离子方程式_________。
已经被氧化的离子方程式_________。
(3)已知![]() 可溶于水,下图表示的是向
可溶于水,下图表示的是向![]() 溶液中逐滴加入
溶液中逐滴加入![]() 溶液时,生成沉淀的物质的量y与加入
溶液时,生成沉淀的物质的量y与加入![]() 的物质的量x的关系。
的物质的量x的关系。
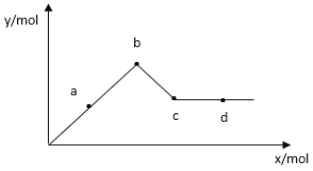
由图可知c点的沉淀是______(填化学式),a-b过程中沉淀物质的量较大的是____(填化学式),写出从开始滴加入![]() 溶液至c点的总反应离子方程式_______。
溶液至c点的总反应离子方程式_______。
【答案】3Fe+8HNO3(稀)=3Fe(NO3)2+2NO↑+4H2O Fe2(SO4)3 KSCN溶液 溶液变为血红色 ![]() BaSO4 BaSO4 2Al3+ + 3SO42- + 3Ba2+ + 8OH- = 3BaSO4 ↓+ 2AlO2- + 4H2O
BaSO4 BaSO4 2Al3+ + 3SO42- + 3Ba2+ + 8OH- = 3BaSO4 ↓+ 2AlO2- + 4H2O
【解析】
(1)Fe过量,与硝酸反应生成硝酸亚铁、NO和水,反应为3Fe+8HNO3=3Fe(NO3)2+2NO↑+4H2O;
(2)亚铁离子易被氧化为铁离子,实验室配制FeSO4溶液时,如果没有隔绝空气,FeSO4会被氧化为Fe2(SO4)3;检验铁离子的溶液用KSCN溶液,铁离子遇到KSCN溶液,溶液显血红色;检验![]() 已经被氧化的离子方程式:Fe3++3SCN-=Fe(SCN)3;
已经被氧化的离子方程式:Fe3++3SCN-=Fe(SCN)3;
(3)在a-b发生反应Al2(SO4)3+3Ba(OH)2=2Al(OH)3↓+3BaSO4↓,c-d发生反应2Al(OH)3+Ba(OH)2=Ba(AlO2)2+4H2O,Al(OH)3溶解,所以c点沉淀只有BaSO4;由方程式Al2(SO4)3+3Ba(OH)2=2Al(OH)3↓+3BaSO4↓可知,沉淀的物质的量:Al(OH)3<BaSO4;
从开始滴加入![]() 溶液至c点,氢氧根过量,铝以偏铝酸根离子形式存在,总反应离子方程式: 2Al3+ + 3SO42- + 3Ba2+ + 8OH- = 3BaSO4 ↓+ 2AlO2- + 4H2O。
溶液至c点,氢氧根过量,铝以偏铝酸根离子形式存在,总反应离子方程式: 2Al3+ + 3SO42- + 3Ba2+ + 8OH- = 3BaSO4 ↓+ 2AlO2- + 4H2O。

 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案【题目】向四支试管中分别加入少量不同溶液进行如下实验,其中操作,现象和结论均正确的是( )
选项 | 操 作 | 现 象 | 结 论 |
A | 先向待测液滴加 | 生成白色沉淀,加酸后沉淀不溶解 | 原溶液中有 |
B | 先向待测液滴加2滴 | 先不显红色,再滴新制的氯水后溶液变为红色 | 原溶液中有 |
C | 用洁净铂丝蘸取溶液进行焰色反应 | 火焰呈黄色 | 原溶液中有 无 |
D | 向待测液滴足量的盐酸 | 将产生的气体通入足量澄清石灰水,溶液变浑浊 | 原溶液中有 |
A.AB.BC.CD.D
【题目】(2011·惠州市调研)一定温度下,难溶电解质AmBn在水中溶解平衡的溶度积为Ksp=cm(An+)×cn(Bm-)。25℃,向AgCl的白色悬浊液中,依次加入等浓度的KI溶液和Na2S溶液,先出现黄色沉淀,最终生成黑色沉淀。已知有关物质的颜色和溶度积如下:
物质 | AgCl | AgI | Ag2S |
颜色 | 白 | 黄 | 黑 |
Ksp(25℃) | 1.8×10-10 | 1.5×10-16 | 1.8×10-50 |
下列叙述不正确的是( )
A.溶度积小的沉淀可以转化为溶度积更小的沉淀
B.若先加入Na2S溶液,再加入KI溶液,则无黄色沉淀产生
C.25℃时,饱和AgCl、AgI、Ag2S溶液中所含Ag+的浓度相同
D.25℃时,AgCl固体在等物质的量浓度的NaCl、CaCl2溶液中的溶度积相同