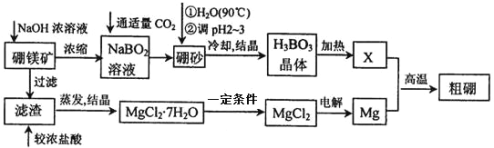
��Ŀ����
����Ŀ��2.48 g��ͭ�Ͻ���ȫ�ܽ���80 mL 4.0 mol��L��1ϡ�����У��õ���״����672 mL NO����(�����ʱ�������������)������˵����ȷ����
A. ȡ��Ӧ����Һ�����뼸��KSCN��Һ����Ѫ��ɫ����
B. �úϽ�������ͭ�����ʵ���֮����1��2
C. ��Ӧ����Һ(������Һ����仯)��c(H��)��2.5 mol��L��1
D. ��Ӧ�����Һ�м���2.0 mol��L��1NaOH��Һ����������ǡ��ȫ������ʱ�������NaOH��Һ�������120 mL
���𰸡�C
��������n(HNO3)=cV=4.0mol/L��0.08L=0.32mol��n(NO)=![]() =
=![]() =0.03mol��
=0.03mol��
�ڸ�������ԭ��Ӧ������ɷֵı仯��4H��+![]() ��2H2O+NO����
��2H2O+NO����
n(H��)(�μӷ�Ӧ)=4n(NO)=0.12mol<n(HNO3)���������������
A. ���������������������ȡ��Ӧ����Һ�����뼸��KSCN��Һ������Ѫ��ɫ����A����B. ���úϽ�������ͭ�����ʵ����ֱ���xmol��ymol����������ɵã�56x+64y=2.48��3x+2y=0.09�����x=0.01��y=0.03���úϽ�������ͭ�����ʵ���֮����1��3����B����C. ��Ӧ����Һ��n(H��)(ʣ��)= n(HNO3)- n(H��)(�μӷ�Ӧ)=0.20mol��c(H��)��![]() =2.5 mol��L��1����C��ȷ��D. ��Ӧ�����Һ�м���2.0 mol��L��1NaOH��Һ���ȷ����кͷ�Ӧ���ٷ���������Ӧ������������ǡ��ȫ������ʱ���γ���������Һ���������Ƶ���ɿɵ�n(HNO3)= n(NaOH)�����Լ���NaOH��Һ�������
=2.5 mol��L��1����C��ȷ��D. ��Ӧ�����Һ�м���2.0 mol��L��1NaOH��Һ���ȷ����кͷ�Ӧ���ٷ���������Ӧ������������ǡ��ȫ������ʱ���γ���������Һ���������Ƶ���ɿɵ�n(HNO3)= n(NaOH)�����Լ���NaOH��Һ�������![]() =160 mL����D����ѡC��
=160 mL����D����ѡC��

 ��У����ϵ�д�
��У����ϵ�д�����Ŀ��80��ʱ��1L �ܱ������г���0.20 mol N2O4��������ӦN2O4![]() 2NO2 ��H = + Q kJ��mol��1(Q��0)������������ݣ�
2NO2 ��H = + Q kJ��mol��1(Q��0)������������ݣ�
ʱ��/s | 0 | 20 | 40 | 60 | 80 | 100 |
c(NO2)/mol��L��1 | 0.00 | 0.12 | 0.20 | 0.26 | 0.30 | 0.30 |
�����ж���ȷ����
A. �����¶ȸ÷�Ӧ��ƽ�ⳣ��K��С
B. 20��40s �ڣ�v(N2O4)= 0.004 mol��L��1��s��1
C. 100sʱ��ͨ��0.40 mol N2O4������ƽ��ʱN2O4��ת��������
D. ��Ӧ��ƽ��ʱ�����յ�����Ϊ0.15Q kJ