题目内容
电池是人类生产、生活中重要的能量来源,各种电池的发明是化学对人类的一项重大贡献。下列有关电池的叙述正确的是
| A.锌锰干电池工作一段时间后碳棒变细 |
| B.氢氧燃料电池可将热能直接转变为电能 |
| C.氢氧燃料电池工作时氢气在负极被氧化 |
| D.太阳能电池的主要材料是高纯度的二氧化硅 |
C
解析试题分析:A、在锌锰干电池中,锌筒是负极,失去电子被氧化。正极是碳棒,该极上二氧化锰发生得电子的还原反应,该电极质量不会减少,故A错误;B、氢氧燃料电池属于原电池的一种,是将化学能转化为电能的装置,不能将热能直接转变为电能,故B错误;C、氢氧燃料电池中,燃料做负极,发生失电子的氧化反应,被氧化,故C正确;D、太阳能电池的主要材料是半导体硅,不是二氧化硅,二氧化硅可以用光导纤维,故D错误,答案选C。
考点:考查常见化学电源工作原理的判断

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
熔融盐燃料电池具有高的发电效率,因而受到重视。用Li2CO3和Na2CO3的熔融盐混合物作电解质,一极通CO气体,另一极通O2和CO2混合气体,可制得在650℃下工作的燃料电池。已知该电池总反应为:2CO+O2=2CO2。则下列说法中正确的是( )
| A.通CO的一极是电池的正极 |
| B.该电池工作过程中需不断补充CO和O2,CO2可循环利用 |
| C.负极反应式为:O2+2CO2+4e-→2CO32- |
| D.正极反应式为:2CO+2CO32-→4CO2+4e- |
如图甲为锌铜原电池装置,乙为电解熔融氯化钠装置。则下列说法正确的是( )
| A.甲装置中锌为负极,发生还原反应 |
| B.甲装置盐桥的作用是使反应过程中ZnSO4溶液和CuSO4溶液保持电中性 |
| C.乙装置中铁极为阳极,电极反应式为: 2Na++2e-=2Na |
| D.乙装置中B是氯气出口,A是钠出口 |
下列各装置中都盛有0.1 mol·L-1的NaCl溶液,放置一定时间后,装置中的四块相同锌片,腐蚀速率由快到慢的正确顺序是
| A.③①④② | B.②①④③ | C.①②③④ | D.①②④③ |
X,Y,Z都是金属,在X与稀H2SO4反应中,加入少量Z的硫酸盐溶液时能使反应加快;X与Y组成原电池时,Y电极质量减少,X,Y,Z三种金属的活动性顺序为:
| A.X>Y>Z | B.X>Z>Y | C.Y>X>Z | D.Y>Z>X |
下列有关金属腐蚀与防护的说法正确的是
| A.纯银器表面在空气中因电化学腐蚀渐渐变暗 |
| B.当镀锡铁制品的镀层破损时,镶层仍能对铁制品起保护作用 |
| C.在海轮外壳连接锌块保护外壳不受腐蚀是采用了牺牲阳极的阴极保护法 |
| D.可将地下输油钢管与外加直流电源的正极相连以保护它不受腐蚀 |
用如图所示装置进行实验,下列叙述不正确的是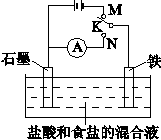
| A.K与N连接时,铁被腐蚀 |
| B.K与N连接时,石墨电极产生气泡 |
| C.K与M连接时,一段时间后溶液的pH增大 |
| D.K与M连接时,石墨电极反应:4OH- - 4e- = 2H2O + O2↑ |
海水淡化的方法有多种,如蒸馏法、电渗析法等。电渗析法是一种利用离子交换膜进行离子交换的方法,其原理如图所示。己知海水中含Na+、Cl—、Ca2+、Mg2+、SO42-等离子,电极为惰性电极。下列叙述中正确的是
| A.B膜是阴离子交换膜 |
| B.通电后,海水中阳离子往a电极处运动 |
| C.通电后,a电极的电极反应式为:4OH--4e-=O2↑+2H2O |
| D.通电后,b电极上产生无色气体,溶液中出现少量白色沉淀 |
