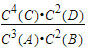题目内容
【题目】下列氧化还原反应方程式(未配平),回答下列问题:
(1)Cl2+KOH——KCl+KClO3+H2O
氧化剂是__________,还原剂是__________,两者的质量之比__________。
(2)在KClO3+HCl(浓)——KCl+Cl2↑+H2O的反应中,当反应中有3 mol电子转移时,产生的Cl2在标准状况下体积是__________。
(3)在KNO3![]() K2O+NO↑+O2↑反应中,氧化产物是___________,还原产物是___________,两者的物质的量之比是___________。
K2O+NO↑+O2↑反应中,氧化产物是___________,还原产物是___________,两者的物质的量之比是___________。
【答案】 Cl2 Cl2 5∶1 40.32 L O2 NO 3∶4
【解析】(1)3Cl2+6KOH![]() 5KCl+KClO3+3H2O中,Cl2自身发生氧化还原反应,生成KCl的反应为被还原的过程,Cl2为氧化剂,生成KClO3的为被还原的过程,Cl2为还原剂,则如有3molCl2参加反应,氧化剂为2.5mol,还原剂为0.5mol,则氧化剂与还原剂的质量之比是2.5:0.5=5:1;(2)在KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O的反应中,每生成3molCl2,转移5mol电子,当反应中有3 mol电子转移时,产生的Cl2在标准状况下体积是V(Cl2)=n(Cl2)·Vm=
5KCl+KClO3+3H2O中,Cl2自身发生氧化还原反应,生成KCl的反应为被还原的过程,Cl2为氧化剂,生成KClO3的为被还原的过程,Cl2为还原剂,则如有3molCl2参加反应,氧化剂为2.5mol,还原剂为0.5mol,则氧化剂与还原剂的质量之比是2.5:0.5=5:1;(2)在KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O的反应中,每生成3molCl2,转移5mol电子,当反应中有3 mol电子转移时,产生的Cl2在标准状况下体积是V(Cl2)=n(Cl2)·Vm=![]() = 40.32 L ;(3)在4KNO3
= 40.32 L ;(3)在4KNO3![]() 2K2O+4NO↑+3O2↑反应中,氧化产物是 O2 ,还原产物是NO,两者的物质的量之比等于方程式中计量数之比,是3∶4。
2K2O+4NO↑+3O2↑反应中,氧化产物是 O2 ,还原产物是NO,两者的物质的量之比等于方程式中计量数之比,是3∶4。

练习册系列答案
相关题目